Дезинфекция колодца марганцовкой самостоятельно
- ПОСЛЕДНИЕ ЗАПИСИ Очистка воды (обратный осмос) Как осушить участок самостоятельно? Как сделать пруд на даче своими руками Делаем пруд на даче своими руками: инструкция по шагам
- РУБРИКИ
- Автоматическое открывание, проветривание и полив теплиц
- Акриловые краски
- Балкон
- Блоки арболитовые
- Бурение скважин на воду
- Вода из скважины
- Водосток кровельный
- Воздух в квартире
- Выращивание дома
- Гидроизоляция
- Гидрофобизация материалов
- Дорожки садовые
- Камин своими руками
- Каркасный дом
- Кладка печи своими руками
- Крыша из металлочерепицы
- МДФ
- Монтаж кровли
- Монтаж ламината
- Монтаж линолеума
- Монтаж подложки под ламинат
- Натяжные потолки
- Опилкобетон
- ОСБ плита
- Отделка откосов
- Оштукатуривание
- Полипропиленовые трубы
- Тротуарная плитка
- Устройство отмостки
- Утепление
- Утепляем баню самостоятельно
- Фасад
- Фундамент из свай
- Шлакоблок
- Эмаль для ванны
Дезинфекция колодца — это обязательное мероприятие с целью очистки колодезной воды, которая со временем приобретает неприятные запах и вкус, вызванные загрязнением. Бактерии и вредоносные организмы заносятся в колодец в период весенних паводков, в результате попадания пыли и грязи, трупов птиц и мелких грызунов, из-за просачивания сточных вод. Причиной могут стать и химикаты, используемые на приусадебных участках для обработки земли или против вредителей.
Бактерии и вредоносные организмы заносятся в колодец в период весенних паводков, в результате попадания пыли и грязи, трупов птиц и мелких грызунов, из-за просачивания сточных вод. Причиной могут стать и химикаты, используемые на приусадебных участках для обработки земли или против вредителей.
Существует множество средств, позволяющих обеззаразить воду, но наиболее востребованным является перманганат калия. Эффективность и безопасность раствора марганцовки проверена временем. Главное, знать не только то, как приготовить средство, но и как правильно провести очистку колодца своими руками.
Проведение дезинфекции колодца
Предполагает выполнение определенной последовательности действий, нарушение которых может привести к повторному засорению и невозможности использования воды для любых бытовых нужд.
Дезинфекция колодезной шахты осуществляется в два этапа:
- подготовительные работы;
- обеззараживающая обработка.
Нельзя приступать к очищению устройства от болезнетворных бактерий и организмов без предварительной подготовки. Иначе эффективность мероприятия будет минимальна.
Иначе эффективность мероприятия будет минимальна.
Подготовка к обеззараживанию
Проводится в следующем порядке:
- Откачка воды. Осуществляется с использованием поверхностного либо погружного насоса. Тип оборудования зависит от уровня колодезной воды, из которой сачком или другим приспособлением с длинной ручкой достают плавающий мусор.
- Замена придонной засыпки. Выполняется с целью предупреждения остатка болезнетворных бактерий. В качестве засыпки допускается применять гравий, песок, щебень. Керамзит лучше не использовать. Он имеет низкий вес и может быть токсичен.
- Устранение трещин.
 Позволяет исключить засорение колодезной воды из-за просачивания грунтовых и сточных вод. Гидроизоляцию проводят специально предназначенными для этого растворами.
Позволяет исключить засорение колодезной воды из-за просачивания грунтовых и сточных вод. Гидроизоляцию проводят специально предназначенными для этого растворами.
Качество выполнения подготовки напрямую влияет на скорость и эффективность дезинфекции в целом.
Приготовление перманганата калия
Использование марганцовки для обеззараживания шахты и колодезной воды обусловлено следующими свойствами этого вещества:
- безопасностью для человека;
- способностью устранять и подавлять патогенные микроорганизмы;
- доступностью и простотой в применении;
- легкостью в смывании.
Чтобы приготовить раствор для дезинфекции, на 10 литров чистой воды кладут 1 чайную ложку перманганата калия. Смесь тщательно перемешивают, применяют по назначению.
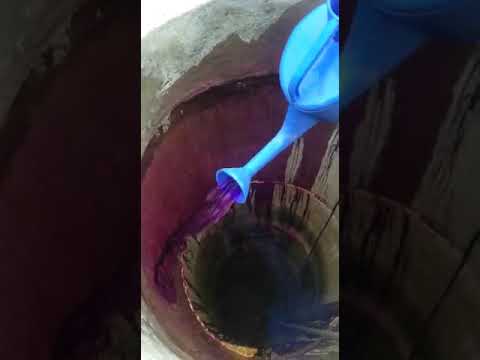
Дезинфекция колодца марганцовкой
Может осуществляться двумя способами:
- Распылением раствора на стены с помощью краскопульта либо другого приспособления.

- Выливанием перманганата калия непосредственно в наполненную водой шахту.
Оба метода предполагают выдерживание колодца закрытым, пока он не заполнится, последующего сливания. Откачку необходимо провести несколько раз. Главное, чтобы вода в колодце стала совершенно чистой.
Чтобы обеззараживание было выполнено максимально качественно, на дно колодца опускают наполненный кремневой крошкой капроновый мешок. Его оставляют внутри даже после выполнения дезинфекции.
Меры предосторожности
Выполнять работы по дезинфекции необходимо с соблюдением нескольких правил:
- работать в паре с помощником для подстраховки;
- обязательно использовать для спуска в шахту крепкую и надежную лестницу;
- не оставаться на дне колодца длительное время.
Марганец, в отличие от белизны и хлорной извести, не выделяет едкого запаха и не разъедает кожу. Обеззараживание с использованием этого раствора можно проводить без респиратора.
Периодичность дезинфекции и использование воды после этого мероприятия
Специалисты рекомендуют обеззараживать колодезную шахту не реже одного раза в полтора-два года либо по мере необходимости. Если вода приобретает плохой запах и вкус, очистку следует провести немедленно. Когда колодец длительное время не эксплуатировался, его использованию обязательно должна предшествовать дезинфекция.
Главным преимуществом применения перманганата калия является то, что воду из колодца после очистки можно пить уже через 24 часа. Когда другого альтернативного источника нет, жидкость перед употреблением первые сутки кипятят. Если используется хлорная известь или белизна, кипячение потребуется проводить 5-10 дней, но полную уверенность в чистоте воды при таком способе дезинфекции позволяет получить только химический анализ.
Заключение
Применение марганцовки представляет собой наиболее безопасный для человека способ дезинфекции колодца, выполняемый собственными силами.
Пренебрегать дезинфекцией нельзя ни в коем случае. Никакие превентивные меры не смогут защитить шахту от попадания и дальнейшего размножения болезнетворных бактерий. Только обеззараживание способно устранить и предупредить размножение этих вредоносных организмов.
Дезинфекция воды из скважины и колодца при автономном водоснабжении/М. Иванов, к.х.н.
Опубликовано: 10 октября 2018 г.
65200
Ухудшение качества воды из автономного источника возможно по разным причинам – затопление в результате весенних паводков, загрязнение при проникновении в источник грунтовых и сточных вод, попадание в воду колодцев и скважин трупов мелких животных и птиц, мелкого мусора и пыли. В любом случае для безопасного водоснабжения из такого источника необходимы процедуры по его очистке, обеззараживании и восстановлении вкусовых качеств воды.
Помимо перечисленных причин на качестве воды в колодце или скважине могут сказаться как чрезмерно интенсивная их эксплуатация, так и длительные перерывы между периодической обработкой. В первом случае при выкачивании воды сверх предусмотренной производительности водо-источника довольно часто происходит проседание грунта. Во втором случае – при длительных сроках эксплуатации без обработки происходит образование на стенках оборудования и сооружений слоёв слизи, грязи, а также солевых и плесневых отложений (рис. 1).
В первом случае при выкачивании воды сверх предусмотренной производительности водо-источника довольно часто происходит проседание грунта. Во втором случае – при длительных сроках эксплуатации без обработки происходит образование на стенках оборудования и сооружений слоёв слизи, грязи, а также солевых и плесневых отложений (рис. 1).
Рис. 1 Слизь и солевые отложения на стенках шахты колодца долго эксплуатировавшегося без обработки
При длительных перерывах в эксплуатации автономных источников, как и при длительных перерывах в их обработке значительно меняются органолептические показатели воды: усиливается окрашивание, появляется запах, понижается прозрачность, а также уменьшается и производительность. Изменение цвета воды может быть вызвано рядом причин (
Рис. 2 Изменение цветности воды из колодца
Так, появление чёрного оттенка воды часто вызвано разложением органических веществ, попавших в источник (рис. 3). Зеленый окрас в большинстве случаев вызван активным размножением в воде водорослей. Желтый цвет у воды появляется при повышении в ней содержания примесей железа.
3). Зеленый окрас в большинстве случаев вызван активным размножением в воде водорослей. Желтый цвет у воды появляется при повышении в ней содержания примесей железа.
Рис. 3 Черный оттенок воды в колодце свидетельствует о разложении попавшей в него органики
Появление у воды из источника запаха и вкуса протухлости может быть вызвано либо редким использованием источника, либо чрезвычайно малым водопотреблением. Понижение прозрачности воды часто вызывается заиливанием, которое возникает при неправильном расположении заборного рукава насоса. В этом случае при работе насоса ил со дна будет взмучиваться и попадать в трубопровод.
Также ухудшению качества воды будет способствовать отсутствие или разрушение глиняного замка источника. Согласно Сан и П 2.1.4.1175-02 «Гигиенические требования к качеству воды нецентрализованного водоснабжения. Санитарная охрана источников» указано, что глиняный замок представляет собой слой хорошо промятой и тщательно уплотнённой глины из жирного суглинка. Этот слой в виде кольца на горизонтальной поверхности имеет толщину в 1 м и глубиной 2 м располагается у оголовка колодца или скважины. Специалисты считают, что такое гидротехническое сооружение предотвратит попадание поверхностных стоков вдоль наружной поверхности ствола в толщу добываемой воды через придонную засыпку.
Этот слой в виде кольца на горизонтальной поверхности имеет толщину в 1 м и глубиной 2 м располагается у оголовка колодца или скважины. Специалисты считают, что такое гидротехническое сооружение предотвратит попадание поверхностных стоков вдоль наружной поверхности ствола в толщу добываемой воды через придонную засыпку.
Любое ухудшение органолептических показателей качества воды может свидетельствовать о том, что такая вода становится опасной для питья. В ней начинают активно развиваться микроорганизмы, которые могут стать причиной различных заболеваний.
Обработка автономных источников воды
Чтобы не качать загрязненную воду из нецентрализованного источника водоснабжения необходимо произвести его обработку в два этапа. На первом этапе следует проводить очистку самого сооружения и оборудования, а на втором – дезинфекцию поступающей в источник воды.
Обработка сооружения в первую очередь включает очистку ствола колодца либо скважины. От тщательности этой предварительной процедуры зависит время дезинфекции и эффективность последующего обеззараживания воды в источнике.
Рис. 4 Откачка воды: а – из колодца, б – из скважины)
Начинается обработка с того, что осуществляется полная откачка воды из колодца или скважины (рис. 4 а, б). Для этой цели целесообразно использовать погружной насос большой мощности. Перед запуском насоса убрать весь плавающий мусор.
Очистка колодца
Если обработке подвергается колодец, то после откачки из него всей воды для визуального осмотра стенок и дна в шахту спускается специалист (рис. 5). В результате осмотра важно выявить наличие в стенках трещин, через которые могут поступать загрязнения. Эти трещины следует герметизировать специальным гидроизолирующим раствором.
Рис. 5 Очистка бетонных поверхностей шахты колодца специалистом
После этого производится очистка внутренней поверхности шахты механическим методом с помощью специального инструмента (щёток, шпателей). В процессе такой очистки с внутренней поверхности ствола необходимо удалять остатки мусора, наросты водорослей частички ила. Кроме этого для очистки бетонных поверхностей используют различные моющие растворы, состав которых зависит от вида преобладающего загрязнения. Так, солевые отложения обычно удаляются с помощью кислотосодержащих моющих растворов. Ими могут быть слабые растворы соляной (HCl) или уксусной (CH3COOH) кислот. При наличии плесневых отложений часто применяют растворы медного купороса (CuSO4). В некоторых случаях на внутренней поверхности шахты колодца, состоящей из бетонных колец, обнаруживаются очаги коррозии. Места, где есть коррозия бетона, следует удалять механическим методом, дабы не позволить ей дальнейшее разрастание.
Кроме этого для очистки бетонных поверхностей используют различные моющие растворы, состав которых зависит от вида преобладающего загрязнения. Так, солевые отложения обычно удаляются с помощью кислотосодержащих моющих растворов. Ими могут быть слабые растворы соляной (HCl) или уксусной (CH3COOH) кислот. При наличии плесневых отложений часто применяют растворы медного купороса (CuSO4). В некоторых случаях на внутренней поверхности шахты колодца, состоящей из бетонных колец, обнаруживаются очаги коррозии. Места, где есть коррозия бетона, следует удалять механическим методом, дабы не позволить ей дальнейшее разрастание.
Рис. 6 Очистка дна колодца
Затем начинают очистку дна колодца (рис. 6), которое сначала очищается от осадка, а затем, по мере возможности, удаляется старая придонная засыпка и засыпается новая. В качестве донной засыпки в большинстве случаев используется мелкая фракция измельченного щебня, гравий или песок. По причине низкого значения насыпной плотности и высокой токсичности не рекомендуется в качестве донной засыпки использовать керамзит.
Очистка скважины
Если для обработки колодцев в большинстве случаев применяют преимущественно механический способ очистки, когда работник спускается в шахту колодца, то для обработки скважины такой подход невозможен из-за меньшего диаметра шахты. Для очистки скважин применяется специальное оборудование. Самым простым способом очистки скважин является откачка воды из нее с помощью специального насоса, который одновременно с водой захватывает песок мусор и камни мелкой фракции. Чтобы такой насос не сломался его периодически следует промывать чистой водой и давать остыть.
Для скважин глубиной до 40 м может быть также применена продувка воздухом под высоким давлением в интервале от 10 атм до 40 атм. Нагнетаемый воздух в виде интенсивного потока пузырей будет выталкивать наружу накопившийся в скважине мусор и очищать поверхность шахты. Однако при такой очистке велика вероятность повреждения скважинного фильтра.
Старые отложения на внутренней поверхности скважины обычно удаляются путем промывки водой (рис. 7), которую также подают под высоким давлением. Отслоившиеся от поверхности шахты загрязнения выносится потоком воды на поверхность через рабочую трубу. Однако и этот способ может стать причиной повреждения фильтра скважины.
7), которую также подают под высоким давлением. Отслоившиеся от поверхности шахты загрязнения выносится потоком воды на поверхность через рабочую трубу. Однако и этот способ может стать причиной повреждения фильтра скважины.
Рис. 7 Промывка скважины
Скважинный фильтр — это фильтр грубой очистки, который препятствует попаданию песка и мелких частиц гравия с размером от 50 до 100 мкм в погружной насос (рис. 8). Даже небольшая степень загрязнения воды механическими примесями приводит к гибели насоса, забивке трубопровода и порче запорной арматуры. Существует несколько видов скважинных фильтров: гравийный, щелевой, сетчатый, перфорированный (дырчатый) и проволочный. Выбор конструкции скважинного фильтра обусловлен характеристиками водоносного слоя, в котором осуществляется водозабор.
Рис. 8 Скважинные фильтры
Для очистки скважин существует и механический способ с помощью желонки (рис. 9).
Рис. 9 Разновидности желонок для механической прочистки скважин
Обыкновенная желонка представляет собой посудину вертикально расположенной цилиндрической формы. В верхней ее части имеется дужка для присоединения к тросу. В нижней части желонки расположен плоский или тарелкообразный клапан в виде поворотного дна. Клапан может поворачиваться вокруг стержня, закрепленного внутри цилиндрической части перпендикулярно ее поверхности. Клапан устроен таким образом, что, когда желонку роняют с большой высоты внутри шахты скважины, ее нижний край вгрызается в загрязнения, а клапан открывается за счет поворота вокруг стержня. При подъеме желонки с помощью троса клапан закрывается, поворачиваясь в горизонтальное положение, и удерживает грязь. За один спуск желонки можно поднять до 0, 5 кг песка и мусора.
В верхней ее части имеется дужка для присоединения к тросу. В нижней части желонки расположен плоский или тарелкообразный клапан в виде поворотного дна. Клапан может поворачиваться вокруг стержня, закрепленного внутри цилиндрической части перпендикулярно ее поверхности. Клапан устроен таким образом, что, когда желонку роняют с большой высоты внутри шахты скважины, ее нижний край вгрызается в загрязнения, а клапан открывается за счет поворота вокруг стержня. При подъеме желонки с помощью троса клапан закрывается, поворачиваясь в горизонтальное положение, и удерживает грязь. За один спуск желонки можно поднять до 0, 5 кг песка и мусора.
Выбор способа очистки шахты скважины производится исходя из ее состояния, и наличия необходимого оборудования.
Дезинфекция воды
После завершения очистки источника водоснабжения приступают непосредственно к дезинфекции воды в нем. Для этой цели применяют химические и физические методы.
Химические методы включают применение дезинфицирующих средств. Наиболее распространенным среди них является хлорная известь, именуемая в народе, как «хлорка». Хлорная известь представляет собой механическую смесь гипохлорита — Ca(ClO) 2, хлорида — CaCl2 и гидроксида кальция — Ca(OH)2. При растворении в воде хлорная известь образует значительную долю рыхлого творожистого осадка белого цвета. Действующим началом в данной смеси является лишь гипохлорит кальция, поскольку в растворе только из него выделяется газообразный хлор, являющийся дезинфицирующим агентом. Поэтому качество хлорной извести и концентрацию дезинфицирующего раствора оценивают по содержанию активного хлора. Продукт достаточно высокого качества содержит от 25 до 30 % активного хлора. Качество хлорной извести может меняться в достаточно сильно в зависимости от времени и условий хранения. Поэтому перед использованием целесообразно проверять активность данного реагента.
Наиболее распространенным среди них является хлорная известь, именуемая в народе, как «хлорка». Хлорная известь представляет собой механическую смесь гипохлорита — Ca(ClO) 2, хлорида — CaCl2 и гидроксида кальция — Ca(OH)2. При растворении в воде хлорная известь образует значительную долю рыхлого творожистого осадка белого цвета. Действующим началом в данной смеси является лишь гипохлорит кальция, поскольку в растворе только из него выделяется газообразный хлор, являющийся дезинфицирующим агентом. Поэтому качество хлорной извести и концентрацию дезинфицирующего раствора оценивают по содержанию активного хлора. Продукт достаточно высокого качества содержит от 25 до 30 % активного хлора. Качество хлорной извести может меняться в достаточно сильно в зависимости от времени и условий хранения. Поэтому перед использованием целесообразно проверять активность данного реагента.
Обычно для обработки используют, так называемое, хлорное молоко, которое готовят путем смешения 1 части хлорной извести с 9 частями воды при интенсивном перемешивании. Этот раствор долго не хранится, теряя свою активность из-за выделяющегося газообразного хлора. Непосредственно перед применением хлорное молоко разводится до концентрации примерно соответствующей 1%-ному раствору хлорной извести.
Этот раствор долго не хранится, теряя свою активность из-за выделяющегося газообразного хлора. Непосредственно перед применением хлорное молоко разводится до концентрации примерно соответствующей 1%-ному раствору хлорной извести.
Активность полученного раствора хлорной извести желательно проверить перед применением. Для этого забирается 3 пробы по 200 мл воды из источника водоснабжения. В первую пробу добавляют 2 капли 1 %-ного раствора, во вторую — 4 капли, в третью — 6 капель. Каждую пробу тщательно перемешивают и выдерживают около 30 мин. По истечению указанного срока все пробы проверяют на присутствие запаха хлора. Останавливаются на пробе, в которой запах хлора едва ощутимый. Используя эмпирическое соотношение, которое гласит, что 25 капель раствора составляют 1 мл, можно рассчитать необходимый объем 1%-ного раствора хлорной извести, который потребуется для обработки полного объема воды в источнике водоснабжения.
Требуемый объем 1 %-ного раствора хлорной извести вносят в воду источника. Желательно, чтобы концентрация активного хлора составляла 75-100 мг/л. После внесения раствора осуществляют интенсивное перемешивание в течение 10 мин любым из доступных способов. В колодце это можно делать путем перемешивание длинным шестом, в скважине при перекачке с помощью насоса, когда заборный и спускной рукава опущены внутрь ствола. После этого источник закрывают непрозрачной пленкой или другим плотным материалом на 6-10 часов в летний период, и от 12 часов до суток в холодное время года. По истечению указанного времени обработки в отобранной пробе воды должен оставаться ощутимый запах хлора. Если он полностью отсутствует, то обработку следует повторить. Если же запах хлорки после выдержки сохранился, то производят откачку воды до тех пор, пока этот запах не исчезнет.
Желательно, чтобы концентрация активного хлора составляла 75-100 мг/л. После внесения раствора осуществляют интенсивное перемешивание в течение 10 мин любым из доступных способов. В колодце это можно делать путем перемешивание длинным шестом, в скважине при перекачке с помощью насоса, когда заборный и спускной рукава опущены внутрь ствола. После этого источник закрывают непрозрачной пленкой или другим плотным материалом на 6-10 часов в летний период, и от 12 часов до суток в холодное время года. По истечению указанного времени обработки в отобранной пробе воды должен оставаться ощутимый запах хлора. Если он полностью отсутствует, то обработку следует повторить. Если же запах хлорки после выдержки сохранился, то производят откачку воды до тех пор, пока этот запах не исчезнет.
Хлорную известь выпускают как отечественные, так и зарубежные производители. Среди отечественных производителей можно отметить ООО «НПО Поволжский завод сорбентов «Татсорб»» (Казань, Татарстан), «Волгоградское ОАО «Химпром» (Волгоград). Из числа зарубежный производителей уместно упомянуть Qingzhou Zhongyuan Chemical Industry Co., Ltd (КНР).
Из числа зарубежный производителей уместно упомянуть Qingzhou Zhongyuan Chemical Industry Co., Ltd (КНР).
Еще одним реагентом для дезинфекции воды в колодцах и скважинах является гипохлорита натрия — Na(ClO)2, который применяется в виде водных растворов. Действующим началом в этом реагенте является активный хлор, содержание которого также, как и в хлорной извести снижается в зависимости от срока хранения.
Водный раствор гипохлорита натрия широко применяется в различных областях, в том числе и в быту как отбеливатель. В розничную продажу он поступает под торговой маркой «Белизна». В этом препарате предельное содержание гипохлорита натрия должно быть не менее 35 %. Одним из производителей этого средства является ООО «Альфа Трейд » (Дзержинск, Нижегородская обл.). Способ применения «Белизны» аналогичен использованию хлорной извести. При обработке воды в колодцах существует эмпирическое правило – на 1 бетонное кольцо диаметром 90 см, заполненного водой, требуется 1 л средства «Белизна». Для скважин справедлива та же пропорция при пересчете на объем обрабатываемой воды.
Для скважин справедлива та же пропорция при пересчете на объем обрабатываемой воды.
В отдельных случаях для дезинфекции воды автономного источника применяют перманганат калия — KMnO4, известный в народе, как «Марганцовка». Эффективность этого средства как дезинфицирующего агента существенно уступает хлорной извести. Но в некоторых случаях применение этого средства может быть оправдано. Для обработки воды в источнике водоснабжения перманганат калия берется из расчета 1 столовая ложка на 10 л воды теплой воды. После тщательного перемешивания раствор выливают в источник водоснабжения. Выдерживают от 30 минут до 1 часа. Перед использованием воду из источника водоснабжения полностью несколько раз откачивают и сливают.
Иногда, в качестве дезинфецирующего средства используют спиртовой раствор йода. Однако, по поводу применения этого средства мнение специалистов расходятся. Одна группа из них считает, что йод является эффективным антибактериальным средством, способным уничтожать патогенные микроорганизмы и препятствовать их размножению в водной среде. В то же время другие специалисты убеждены, что необходимая концентрация йода, обладающая надежным бактерицидным действием, сделает воду из источника непригодную для питья и полива растений.
В то же время другие специалисты убеждены, что необходимая концентрация йода, обладающая надежным бактерицидным действием, сделает воду из источника непригодную для питья и полива растений.
Наряду с перечисленными способами дезинфекции воды в источнике к химическим методам можно отнести и применение дозирующих патронов. Это приспособление представляет собой цилиндрические трубки длиной до 1 м и диаметром от 50 до 100 мм, изготовленные из пористого керамического материала. Внутри дозирующего патрона имеется полость емкостью от 250 до 1000 мл, которая заполняется дезинфицирующим реагентом, например, гипохлоритом натрия. Дозирующий патрон, заполненный дезинфицирующим хлорсодержащим средством, на 30 дней опускается с помощью троса в источник водоснабжения. За это время из патрона хлор дозированно выделяется в воду источника дезинфицируя ее.
Помимо перечисленного, на российском рынке дезинфицирующих средств для обработки воды имеется ряд хлорсодержащих препаратов в таблетках: «Акватабс» (производитель «Медентек Лтд», Ирландия), «Аквабриз» и другие.
Активным веществом в таблетках «Акватабс» и «Аквабриз» является натриевая соль дихлоризоциануровой кислоты (Na-соли ДХЦК) . Для «Аквабриз» действующее вещество поставляется из Китая, где производится на предприятии «Сянь-Хань Лтд.» в провинции Чуньджунь.
Таблетки «Акватабс» предназначены для обеззараживания питьевой воды. Однако, дозировка активного вещества больше соответствует количествам воды, применяемой в быту, а не для дезинфекции скважин и колодцев (табл.). Так, таблетки «Акватабс» выпускаются 4 видов, в зависимости от различного содержания Na-соли ДХЦК.
Таблица. Содержание натриевой соли дихлоризоциануровой кислоты в таблетках «Акватабс»
|
Наименование таблетки |
Содержание натриевой соли ДХЦК в каждой таблетке, мг |
Содержание активного хлора в таблетке, мг |
|---|---|---|
|
Акватабс 3,5 |
3, 5 |
2,0 |
|
Акватабс 3,5 |
8, 5 |
5,0 |
|
Акватабс 3,5 |
12, 5 |
7,3 |
|
Акватабс 3,5 |
17, 0 |
10,0 |
Для воды из колодца и скважины в количестве 1 л требуется 1 таблетка, содержащая 20 мг активного хлора. При этом величина остаточного свободного хлора составляет 0,3- 0,5 мг/л.
При этом величина остаточного свободного хлора составляет 0,3- 0,5 мг/л.
Средство «Аквабриз» (таблетки) производства ООО «Мир дезинфекции» (Москва) также предназначено для обеззараживания питьевой воды. В качестве действующего вещества присутствует та же соль- Nа-соль ДХЦК. Одновременно с этим в таблетках присутствуют также бикарбонат натрия, хлорид натрия, адипиновая кислота. Средство «Аквабриз» выпускается в таблетках в виде 8-ми готовых форм, различающихся по содержанию Nа-соль ДХЦК: 3, 6 мг, 4, 5 мг, 18 0 мг, 0, 5 г, 0,9 г; 1,8 г; 3,0 г; 8,9 г. Эти дозировки активного вещества соответствуют следующим концентрациям активного хлора: 2,0 мг; 2,5 мг; 10,0 мг; 300 мг; 750мг; 1000 мг; 1670мг; 5000 мг.
Для обработки значительных объемов воды, таких как в колодцах или скважинах, рекомендованы следующие препараты «Аквабриз 300», «Аквабриз «750», «Аквабриз 1000», «Аквабриз 1670», «Аквабриз 5000». Индекс в маркировке указывает на содержание в таблетках активного хлора, выраженного в мг. Для дезинфекции воды из артезианских скважин и защищенных колодцев рекомендуется применять 1 таблетку «Аквабриз 5000» из расчета на 1250 л обрабатываемой воды. Для колодцев, у которых отсутствуют защитные укрытия рекомендовано применять данный препарат из расчета одна таблетка «Аквабриз 5000» на 1 м3. Во всех случаях время выдержки после введения в воду препарата около 60 мин. Гарантированное время действия дезинфекционной обработки в зависимости от внешних факторов может колебаться от 10 суток до 1 месяца.
Для дезинфекции воды из артезианских скважин и защищенных колодцев рекомендуется применять 1 таблетку «Аквабриз 5000» из расчета на 1250 л обрабатываемой воды. Для колодцев, у которых отсутствуют защитные укрытия рекомендовано применять данный препарат из расчета одна таблетка «Аквабриз 5000» на 1 м3. Во всех случаях время выдержки после введения в воду препарата около 60 мин. Гарантированное время действия дезинфекционной обработки в зависимости от внешних факторов может колебаться от 10 суток до 1 месяца.
По сравнению с хлорной известью и средством «Белизна» химические препараты в таблетках имеют некоторые преимущества: высокую степень обеззараживания, удобство при приготовлении раствора, меньшее время выдержки при обработке и безопасность в использовании.
К физическим методам дезинфекции относится ультразвуковая и ультрафиолетовую (УФ) обработку воды. Основой УФ-дезинфекции воды является применение УФ-ламп с максимумом излучения при 254 нм, который характеризуется наибольшей дезинфицирующей способностью (рис. 10). Для дезинфекции воды, выкачиваемой из колодца либо скважины наиболее удобны приборы, работающие в проточном режиме. Современные модели такого оборудования оснащаются электронным блоком управления, который автоматически регулирует подачу воды.
10). Для дезинфекции воды, выкачиваемой из колодца либо скважины наиболее удобны приборы, работающие в проточном режиме. Современные модели такого оборудования оснащаются электронным блоком управления, который автоматически регулирует подачу воды.
Рис. 10 Ультрафиолетовый стерилизатор для дезинфекции воды в скважине.
Одним из производителей установок для УФ-обеззараживания воды является международный концерн BWT (Германия). Она выпускает устройства для проведения облучения воды серии «Bewades». Такие приборы характеризуются дозой облучения 40 мДж/см², что позволяет их применять для облучения питьевой воды. В них установлены лампы фирмы Philips (Голландия) с продолжительностью работы 11000 — 14000 час.
УФ-установки серии «Блеск», выпускающиеся отечественным производителем «Национальные водные ресурсы» (Москва), способны проводить обработку воды с производительностью от 1, 0 до 50 м3/час. В них также установлены УФ-лампы фирмы Philips. Еще одним известным отечественным продуктом являются установки серии «Бакт» с производительностью по воде от 0, 3 до 5,0 м3/час. Их выпускает компания «Бактерицидные Технологии» (Мытищи, Московская область).
Их выпускает компания «Бактерицидные Технологии» (Мытищи, Московская область).
При ультразвуковой дезинфекции оборудование излучает волны в ультразвуковом диапазоне, которые также вызывают гибель микроорганизмов. Одной из компаний, предлагающих оборудование для обеззараживание питьевой воды ультразвуком в проточном режиме с величиной потока от 1, 0 м3/ час является «Новотех-Эко» (Вологда).
Физические методы дезинфекции воды обладают достаточно высокой эффективностью и экологической безопасностью. Однако для их осуществления необходимо использование весьма дорогостоящего оборудования. Устанавливать такое оборудование оправдано в том случае, если водоснабжение необходимо для домов с круглогодичным проживанием.
Cтатья из журнала «Аква-Терм» № 5/2018, рубрика «Водоснабжение и водоподготовка».
Статьи
Поделиться:вернуться назад
Полимерный воздухоподогреватель HeatMatrix ООО «АЛВАС Инжиниринг»
Экспертиза системы отопления: когда, зачем и как проводится
IE4 или IE5: будущее все ближе
Водоснабжение из скважины
Очистка питьевой воды – Перманганат калия – Питьевая вода и здоровье человека
ЭФФЕКТИВНО ПРОТИВ: Растворенного железа и марганца, сероводорода.
Содержимое
|
Использование перманганата калия
Перманганат калия представляет собой метод очистки на входе, который окисляет растворенное железо, марганец и сероводород в твердые частицы, которые отфильтровываются из воды. Его также можно использовать для контроля роста железосодержащих бактерий в скважинах.
Как работает перманганат калия
Перманганат калия доступен в виде сухого пурпурного твердого вещества. Устройство впрыскивает раствор перманганата калия в воду между водяным насосом и накопительным баком.
Перманганат калия окисляет железо, марганец и сероводород до частиц. Затем частицы фильтруются с помощью мультимедийного фильтра, который может представлять собой либо алюмосиликат, покрытый марганцем, поверх обработанного марганцем зеленого песка, либо 8-дюймовый слой антрацита поверх обработанного марганцем зеленого песка. Если перед фильтрацией окисляется недостаточное количество железа, марганца или сероводорода, марганцевое покрытие на фильтрующем материале действует как резервный окислитель для обработки любого оставшегося загрязнения. Если перед фильтрацией в воду подается слишком много перманганата калия, избыток перманганата калия служит регенерантом фильтрующего материала. Вода на выходе из фильтра должна быть бесцветной.
Затем частицы фильтруются с помощью мультимедийного фильтра, который может представлять собой либо алюмосиликат, покрытый марганцем, поверх обработанного марганцем зеленого песка, либо 8-дюймовый слой антрацита поверх обработанного марганцем зеленого песка. Если перед фильтрацией окисляется недостаточное количество железа, марганца или сероводорода, марганцевое покрытие на фильтрующем материале действует как резервный окислитель для обработки любого оставшегося загрязнения. Если перед фильтрацией в воду подается слишком много перманганата калия, избыток перманганата калия служит регенерантом фильтрующего материала. Вода на выходе из фильтра должна быть бесцветной.
При очистке воды от железобактерий в скважину подается раствор перманганата калия. Было обнаружено, что концентрация от 3,8 до 7,6 граммов на галлон очень эффективна. После добавления раствора в лунку непрерывное перемешивание поможет разрыхлить и разрушить осадок и органический материал, вырабатываемый бактериями, что повысит эффективность очистки. Перемешивание можно осуществить, включив и выключив колодец, в результате чего вода поднимается через обсадную трубу колодца, а затем позволяет ей падать обратно в колодец.
Перемешивание можно осуществить, включив и выключив колодец, в результате чего вода поднимается через обсадную трубу колодца, а затем позволяет ей падать обратно в колодец.
Техническое обслуживание устройства с перманганатом калия
Запасы перманганата калия необходимо периодически пополнять в рамках регламентного обслуживания. При использовании перманганата калия в скважине также может потребоваться периодическая обработка для растворения отложений железа и минеральной накипи. Такая обработка требует использования сильных кислот, поэтому обратитесь за консультацией к специалисту по очистке воды. Устройства и насосы для впрыска перманганата калия аналогичны тем, которые используются в системах хлорирования.
Особые указания по использованию перманганата калия
Использование перманганата калия требует тщательной калибровки, технического обслуживания и контроля. Перманганат калия чувствителен к экстремальным температурам и лучше всего работает при температуре от 50 до 72 градусов по Фаренгейту. Колодезная вода примерно 55 градусов по Фаренгейту.
Колодезная вода примерно 55 градусов по Фаренгейту.
Перманганат калия ядовит и вызывает раздражение кожи, поэтому обращайтесь с ним осторожно и следите за тем, чтобы в очищенной воде не было избытка перманганата калия. Химическое вещество придает воде легкий розовый оттенок. После обработки вода должна быть бесцветной. Концентрированное химическое вещество должно храниться в оригинальной упаковке, в недоступном для детей и животных месте. Защищайте контейнеры для хранения от физических повреждений.
Вопросы, которые следует задать перед покупкой
Перед покупкой устройства для очистки воды проверьте воду в сертифицированной государственной лаборатории на наличие загрязняющих веществ. Это поможет вам определить, является ли перманганат калия эффективным методом лечения в вашей ситуации. Дополнительные сведения см. в разделе Вопросы, которые необходимо задать перед покупкой системы очистки воды.
Адаптировано из: Wagenet, L., K. Mancl, and M. Sailus. (1995). Домашняя очистка воды. Северо-восточная региональная служба сельскохозяйственного машиностроения, Кооперативное расширение. НРАЭС-48. Итака, Нью-Йорк.
(1995). Домашняя очистка воды. Северо-восточная региональная служба сельскохозяйственного машиностроения, Кооперативное расширение. НРАЭС-48. Итака, Нью-Йорк.
Очистка перманганатом калия является эффективным гигиеническим методом снижения бактериальной биологической нагрузки на сырье Coriandrum sativum | Заметки об исследованиях BMC
- Заметки об исследованиях
- Открытый доступ
- Опубликовано:
- Супрам Хосуру Субраманья ORCID: orcid.org/0000-0002-3488-4217 1 ,
- Васудха Пай 2 ,
- Индира Бэри 2 , 9001 2 Ниранджан Наяк 1 ,
- Шишир Гокхале 1 и
- …
- Бриджеш Сатьян 1
Исследовательские заметки BMC том 11 , Номер статьи: 124 (2018) Процитировать эту статью
32 тыс.
 обращений
обращений8 цитирований
15 Альтметрический
Детали показателей
Abstract
Objective
Сырые овощи, включая цветы, листья, стебли и корни, являются важными переносчиками пищевых патогенов. Оценивали бактериологическую обсемененность немытых листьев кориандра и эффективность очистки 0,1% раствором перманганата калия как метода обеззараживания.
Результаты
Значительное бактериальное загрязнение, включая такие патогены, как 9Из немытых листьев кориандра было выделено 0058 видов Salmonella и видов Aeromonas . Обеззараживание 0,1% раствором перманганата калия оказалось более эффективным, чем трехступенчатая промывка стерильной водой.
Обеззараживание 0,1% раствором перманганата калия оказалось более эффективным, чем трехступенчатая промывка стерильной водой.
Введение
Вспышки болезней пищевого происхождения увеличиваются во всем мире, листовая зелень является общепризнанным потенциальным источником бактериальных инфекций пищевого происхождения [1]. Безопасность пищевых продуктов имеет большое значение для здоровья человека. Потребление свежих, сырых или частично приготовленных овощей играет важную роль во вспышках инфекций пищевого происхождения [2, 3]. Безопасность потребления листовых зеленых овощей вызывает все большую озабоченность, особенно в развивающихся странах. Они могут быть загрязнены во время выращивания, транспортировки и хранения [2,3,4]. В недавнем отчете совещания ФАО/ВОЗ 2007 г. был представлен обзор патогенов, наиболее часто встречающихся в свежих фруктах и овощах (http://www.who.int/foodsafety). Свежие овощи и травы были вовлечены в передачу микробных инфекций пищевого происхождения по всему миру [3]. Вспышка шига-токсина, производящего 9Инфекции 0058 Escherichia coli , связанные с потреблением листовых овощей, вызвали почти 200 лабораторно подтвержденных заболеваний, 100 госпитализаций и несколько смертей в США в 2006 г. [5]. В то время как листовые овощи являются важной частью здорового питания, потребление сырых загрязненных ароматизаторов вызывает серьезную озабоченность.
Вспышка шига-токсина, производящего 9Инфекции 0058 Escherichia coli , связанные с потреблением листовых овощей, вызвали почти 200 лабораторно подтвержденных заболеваний, 100 госпитализаций и несколько смертей в США в 2006 г. [5]. В то время как листовые овощи являются важной частью здорового питания, потребление сырых загрязненных ароматизаторов вызывает серьезную озабоченность.
Дезинфекция важна для дезинфекции зеленых листовых овощей и фруктов. Многие исследователи обнаружили эффективность различных дезинфицирующих средств для снижения биологической нагрузки на готовую к употреблению листовую зелень. Известно, что перманганат калия (KMnO 4 ) является одним из таких эффективных дезинфицирующих средств, и многие исследователи использовали его против широкого спектра микроорганизмов. Сориано и др. [6] и Amoah et al. [7] использовали раствор перманганата калия для дезинфекции салата и обнаружили значительное снижение бактериальной нагрузки на эти зеленые листья. Как и листья салата, кориандр или кинза ( Coriandrum sativum ) — очень часто используемые съедобные листья, которыми часто украшают приготовленные блюда. Кроме того, он является деликатесом в большинстве азиатских блюд из-за его уникального вкуса. Таким образом, мы планировали изучить микробное качество листьев кориандра, поскольку эти листья в сыром виде могут быть контаминированы одним или несколькими патогенными микроорганизмами. Промывание простой водой перед использованием, как это делается во многих домашних кулинарных практиках, не может гарантировать отсутствие патогенов. Таким образом, представляется необходимым обеззараживать листья кориандра перед употреблением в пищу. Это исследование было проведено для определения микробиологического качества сырых листьев кинзы и оценки эффективности промывки 0,1% KMnO 9.Раствор 0146 4 для обеззараживания.
Как и листья салата, кориандр или кинза ( Coriandrum sativum ) — очень часто используемые съедобные листья, которыми часто украшают приготовленные блюда. Кроме того, он является деликатесом в большинстве азиатских блюд из-за его уникального вкуса. Таким образом, мы планировали изучить микробное качество листьев кориандра, поскольку эти листья в сыром виде могут быть контаминированы одним или несколькими патогенными микроорганизмами. Промывание простой водой перед использованием, как это делается во многих домашних кулинарных практиках, не может гарантировать отсутствие патогенов. Таким образом, представляется необходимым обеззараживать листья кориандра перед употреблением в пищу. Это исследование было проведено для определения микробиологического качества сырых листьев кинзы и оценки эффективности промывки 0,1% KMnO 9.Раствор 0146 4 для обеззараживания.
Основной текст
Материалы и методы
Всего было закуплено 35 связок листьев кориандра у 35 продавцов, работающих на 17 различных овощных рынках, расположенных по всему городу Удупи, Индия. Образцы были собраны в ходе двадцати посещений поставщиков в течение полутора месяцев с февраля по март 2016 года. Образцы были собраны в предварительно стерилизованные пластиковые пакеты и с минимальной задержкой доставлены в микробиологическую лабораторию. Корни образца обрезали в асептических условиях, а листья и части стебля измельчали стерильными ножницами. Измельченные листья затем делили на аликвоты на 3 порции A, B и C, каждая весом приблизительно 25–30 г. Они обрабатывались отдельно.
Образцы были собраны в ходе двадцати посещений поставщиков в течение полутора месяцев с февраля по март 2016 года. Образцы были собраны в предварительно стерилизованные пластиковые пакеты и с минимальной задержкой доставлены в микробиологическую лабораторию. Корни образца обрезали в асептических условиях, а листья и части стебля измельчали стерильными ножницами. Измельченные листья затем делили на аликвоты на 3 порции A, B и C, каждая весом приблизительно 25–30 г. Они обрабатывались отдельно.
Часть А измельченных листьев инокулировали в бульон селенита F (примерно 20–25% по объему) и инкубировали при 37 °C в течение 6 ч для обогащения фекальными патогенами, такими как видов Salmonella и видов Shigella [8]. Полную петлю бульона селенита F субкультивировали на ксилозо-лизин-дезоксихолатном агаре и исследовали через 14–18 часов инкубации при 37 °C. Колонии, представляющие видов Salmonella или видов Shigella , были дополнительно изучены и охарактеризованы морфологически и биохимически с помощью автоматизированной системы VITEK [8].
Часть B образцов была проанализирована количественно на общее количество путем добавления 50 мл стерильной дистиллированной воды и ручного встряхивания в течение 3 минут со скоростью примерно 20 встряхиваний в минуту. Содержимое промывной воды (вода) подвергали серийному десятикратному разведению (1:10–1:10 000 в стерильной пептонной воде) и 0,01 мл объема чистого раствора, и каждое разведение инокулировали на чашки с агаром МакКонки для определения КОЕ/мл образец. Процесс промывки повторяли три раза и аналогичным образом инокулировали содержимое воды. Все чашки инокулировали при 37 °C в течение 18–24 часов. Общий бактериологический подсчет регистрировали во время каждого процесса промывки. Различные морфотипы бактерий далее идентифицировали с помощью стандартных биохимических реакций [8].
Часть C погружали в 0,1% раствор перманганата калия (KMnO 4 ) при ручном встряхивании со скоростью приблизительно 20 встряхиваний в минуту, обеспечивая в общей сложности 10 минутное время контакта при комнатной температуре. Раствор декантировали, к листьям добавляли свежую стерильную дистиллированную воду и декантировали для удаления следов KMnO 4 . Повторно наполненную свежую воду энергично встряхивали и использовали для определения количества колоний, применяя ту же процедуру, что и указанная выше для порции B. Все эксперименты проводились в двух повторностях и при комнатной температуре приблизительно 23 °C.
Раствор декантировали, к листьям добавляли свежую стерильную дистиллированную воду и декантировали для удаления следов KMnO 4 . Повторно наполненную свежую воду энергично встряхивали и использовали для определения количества колоний, применяя ту же процедуру, что и указанная выше для порции B. Все эксперименты проводились в двух повторностях и при комнатной температуре приблизительно 23 °C.
Анализ данных
Полученные данные были проанализированы с помощью программного обеспечения IBM SPSS Statistics 20 от IBM Corporation, Армонк, Нью-Йорк, США. 95% доверительный интервал, используемый для обобщения всех средних значений. Жизнеспособные количества были нормализованы логарифмическим преобразованием перед применением t-критерия для сравнения с исходным уровнем. значение р<0,05 считается статистически значимым.
Результаты
Salmonella typhi была выделена из одного образца части А (1/35). В части B все 35 образцов показали бактериальное загрязнение со средним числом жизнеспособных микроорганизмов 1,6 × 10 7 КОЕ/мл (7,2 log10 КОЕ/мл). Во всех пробах обнаружены грамотрицательные бактерии группы кишечной палочки. Непредвиденные обстоятельства в Таблице 1 показывают количество и процент выделения различных бактерий. Потенциальный патоген Aeromonas spp. были обнаружены в 6 (17%) пробах. Из 95% (33/35) проб были выделены два и более вида бактерий. Этапы промывки части B водой показали среднее снижение жизнеспособной бактериальной нагрузки на 1,2 log во время первой промывки, за которым последовало снижение на 1,9 log после второй промывки и на 3,4 log после третьей промывки. По сравнению с данными, полученными в части B, количество жизнеспособных клеток в части C (KMnO 4 стирка) уменьшилась на 4,1 лог. Логарифм снижения биологической нагрузки на каждой стадии промывки водой и одной стадии обеззараживания перманганатом калия показан на рис. 1. Рис. 1
Во всех пробах обнаружены грамотрицательные бактерии группы кишечной палочки. Непредвиденные обстоятельства в Таблице 1 показывают количество и процент выделения различных бактерий. Потенциальный патоген Aeromonas spp. были обнаружены в 6 (17%) пробах. Из 95% (33/35) проб были выделены два и более вида бактерий. Этапы промывки части B водой показали среднее снижение жизнеспособной бактериальной нагрузки на 1,2 log во время первой промывки, за которым последовало снижение на 1,9 log после второй промывки и на 3,4 log после третьей промывки. По сравнению с данными, полученными в части B, количество жизнеспособных клеток в части C (KMnO 4 стирка) уменьшилась на 4,1 лог. Логарифм снижения биологической нагрузки на каждой стадии промывки водой и одной стадии обеззараживания перманганатом калия показан на рис. 1. Рис. 1
Количество жизнеспособных бактерий листьев кориандра после стерильной воды и KMnO 4 промывка
Изображение в полный размер
Обсуждение
Потребление сырых фруктов и овощей связано с несколькими заболеваниями пищевого происхождения [9, 10]. В развивающихся странах неочищенные сточные воды орошения и навоз в качестве удобрений способствуют загрязнению овощей и трав фекальной флорой человека и животных [11]. Если во время транспортировки и хранения не соблюдается холодовая цепь, может произойти размножение бактерий. Несколько исследований продемонстрировали наличие потенциальных патогенов на свежих овощах и листьях [3, 7, 11]. В этом исследовании мы продемонстрировали заражение кинзы различными фекальными флорами, которые могут колонизировать или вызывать инфекцию у людей. Обнаружение кишечных патогенов типа Salmonella spp., Aeromonas spp. и Escherichia coli вызывает серьезную озабоченность. Листья могли быть заражены на фермах во время выращивания, вероятно, из-за орошения сточными водами. Mritunjay и Kumar [12] сообщили о заражении овощных салатов такими патогенами, как Salmonella и Enterohaemorrhagic Escherichia coli. Они считали, что кишечные бактерии будут размножаться в отсутствие эффективных мер по обеззараживанию во время сбора, обработки и упаковки.
В развивающихся странах неочищенные сточные воды орошения и навоз в качестве удобрений способствуют загрязнению овощей и трав фекальной флорой человека и животных [11]. Если во время транспортировки и хранения не соблюдается холодовая цепь, может произойти размножение бактерий. Несколько исследований продемонстрировали наличие потенциальных патогенов на свежих овощах и листьях [3, 7, 11]. В этом исследовании мы продемонстрировали заражение кинзы различными фекальными флорами, которые могут колонизировать или вызывать инфекцию у людей. Обнаружение кишечных патогенов типа Salmonella spp., Aeromonas spp. и Escherichia coli вызывает серьезную озабоченность. Листья могли быть заражены на фермах во время выращивания, вероятно, из-за орошения сточными водами. Mritunjay и Kumar [12] сообщили о заражении овощных салатов такими патогенами, как Salmonella и Enterohaemorrhagic Escherichia coli. Они считали, что кишечные бактерии будут размножаться в отсутствие эффективных мер по обеззараживанию во время сбора, обработки и упаковки. Диареогенный потенциал E coli , полученная в нашем случае, не могла быть определена из-за нехватки ресурсов. E coli Q157:H7 может выживать в сырых овощах при температуре окружающей среды, сохраняя свою инфекционность. Серьезные заболевания, начиная от кровавой диареи и заканчивая гемолитико-уремическим синдромом, могут возникать из-за употребления зараженных сырых овощей [13].
Диареогенный потенциал E coli , полученная в нашем случае, не могла быть определена из-за нехватки ресурсов. E coli Q157:H7 может выживать в сырых овощах при температуре окружающей среды, сохраняя свою инфекционность. Серьезные заболевания, начиная от кровавой диареи и заканчивая гемолитико-уремическим синдромом, могут возникать из-за употребления зараженных сырых овощей [13].
В этом исследовании Pseudomonas aeruginosa, Providenia spp. , Morganella spp. и Serretia spp. были обнаружены среди 11,42, 5,71, 2,87 и 8,57% экземпляра соответственно. Майкл и др. [14] также сообщили об этих организмах в сырых овощах. Pseudomonas aeruginosa , являясь обычным естественным обитателем почвы, может контаминировать овощи. Morganella и Providencia , будучи частью нормальной флоры желудочно-кишечного тракта человека и животных, могут загрязнять почву при дефекации в открытом грунте. Эти условно-патогенные микроорганизмы могут вызывать септицемию у лиц с ослабленным иммунитетом.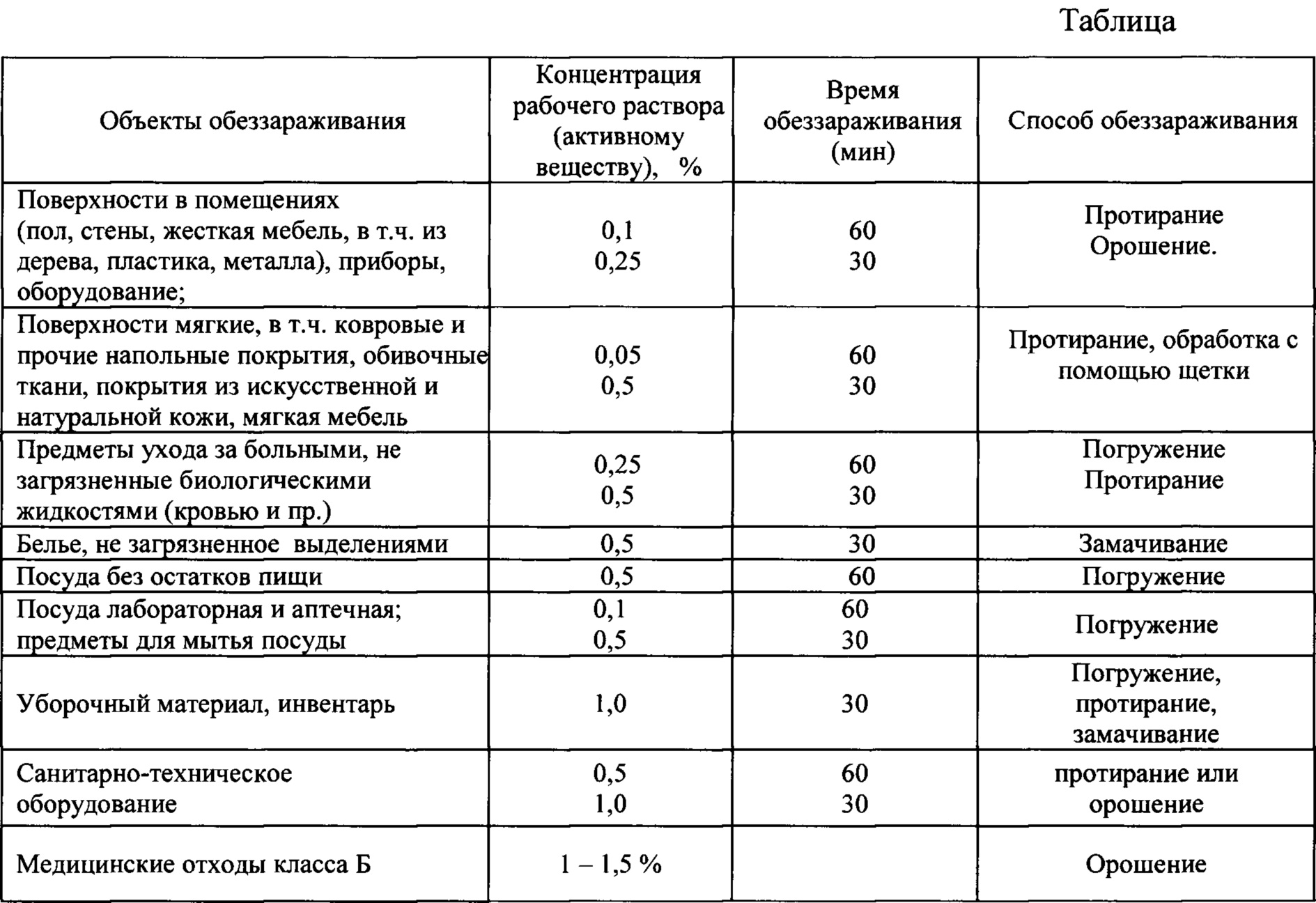 Поэтому внимание должно быть сосредоточено на обработке, хранении и транспортировке пищевых продуктов, чтобы устранить потенциальные патогены.
Поэтому внимание должно быть сосредоточено на обработке, хранении и транспортировке пищевых продуктов, чтобы устранить потенциальные патогены.
Мытье листовых овощей водой, предназначенной для вымывания микроорганизмов, считается удовлетворительным методом дезинфекции в домашних условиях. Но на этот метод влияют различные факторы, такие как наличие достаточного количества чистой воды и первоначальная бионагрузка на продукты питания. Показано, что многократное промывание водой значительно снижает бионагрузку [7], только когда этапы промывания многократны, строги и энергичны. В настоящем исследовании, а также в аналогичном исследовании, проведенном ранее [6], для начального этапа промывки использовалась стерильная дистиллированная вода, что может показаться не идеальным методом, поскольку это может привести к повреждению бактериальных клеток. Однако такое начальное воздействие стерильной дистиллированной воды в течение очень ограниченного периода времени могло не повлиять на качество результата.
Многие исследователи работали над эффективностью различных дезинфицирующих и обеззараживающих средств, таких как растворы NaCl, уксус, смесь соли и уксуса, стиральный порошок, бытовые отбеливатели, йод, тринатрийфосфат и т. д. в различных концентрациях и с разным временем контакта, но ни одно из них может полностью устранить фекальные колиформные популяции из овощей и фруктов [9].
Из доступных методов обеззараживания листовой зелени хлорирование считается эффективным, но оно влияет на структурную целостность листьев. Эффективность обычного отбеливателя изменчива и ненадежна. Гамма-облучение в малых дозах было еще одним методом, который эффективно снижал микробную нагрузку при сохранении качества листовых овощей, употребляемых в сыром виде [15].
Известно, что раствор перманганата калия снижает количество патогенных бактерий и паразитов на свежих овощах и фруктах [7, 16, 17]. В этом исследовании мы наблюдали, что жизнеспособная бактериальная нагрузка на кинзу была значительно снижена при промывании KMnO 4 .
KMnO 4 в малых концентрациях часто используется в качестве антисептического ополаскивателя для поддержания гигиены полости рта, а также как очиститель колодезной воды, используемой для питья. Согласно последним рекомендациям ВОЗ, KMnO 4 в такой низкой концентрации, как 1:10 000, может быть безопасным для местного применения на открытые раны [18, 19], при этом летальный эффект достигается далеко друг от друга, что соответствует дозе до 10 г [20]. Таким образом, мытье пищевых продуктов очень низкой концентрацией (0,1%) раствора KMnO 4 с последующей промывкой простой водой может не оказывать неблагоприятного воздействия на здоровье человека.
Роль образования, обучения и информирования производителей, обработчиков и потребителей важна для повышения безопасности продукции. Мытье овощей перед употреблением — важный подход к снижению риска для здоровья. Это исследование показало, что листья кориандра имеют высокое бактериальное загрязнение, в том числе такие патогены, как 9. 0058 Salmonella spp. , Aeromonas spp. и E coli . Обеззараживающее действие раствора перманганата калия на листья оказалось лучше, чем три этапа промывки простой водой. Влияние раствора KMnO 4 на здоровье человека и вкус или аромат листьев в данной работе не изучалось; это подчеркнуло необходимость дальнейших исследований в определенных областях для облегчения эффективного санитарного метода.
0058 Salmonella spp. , Aeromonas spp. и E coli . Обеззараживающее действие раствора перманганата калия на листья оказалось лучше, чем три этапа промывки простой водой. Влияние раствора KMnO 4 на здоровье человека и вкус или аромат листьев в данной работе не изучалось; это подчеркнуло необходимость дальнейших исследований в определенных областях для облегчения эффективного санитарного метода.
Заключение
В данной работе подчеркивается бактериальное разнообразие и нагрузка на сырые листья кориандра. Раствор перманганата калия с концентрацией 0,1% при минимальном времени контакта 10 минут оказался эффективным и простым методом значительного снижения бактериальной нагрузки. Это может быть использовано в качестве альтернативы или в сочетании с промывкой простой водой. Насколько нам известно, это первое в истории исследование, демонстрирующее эффективность раствора перманганата калия в качестве очищающего средства для кинзы.
Ограничение
В этом исследовании участвуют только бактерии, культивируемые in vitro. Бактериальные изоляты не были дополнительно охарактеризованы в отношении свойств вирулентности или лекарственной устойчивости. Эффективность промывки KMnO 4 тестировали для разовой концентрации и времени контакта.
Бактериальные изоляты не были дополнительно охарактеризованы в отношении свойств вирулентности или лекарственной устойчивости. Эффективность промывки KMnO 4 тестировали для разовой концентрации и времени контакта.
Сокращения
- КМНО 4 :
перманганат калия
- ФАО:
Продовольственная и сельскохозяйственная организация Объединенных Наций
- ВОЗ:
Всемирная организация здравоохранения
- КОЕ:
колониеобразующие единицы
- NaCl:
натрия хлорид
Ссылки
- «>
ФАО/ВОЗ. Серия оценок микробиологического риска 14: микробиологическая опасность свежих листовых овощей и зелени. 2008б. ftp://ftp.fao.org/docrep/fao/011/i0452e/i0452e00.pdf. По состоянию на 15 октября 2017 г.
Painter JA, et al. Отнесение болезней пищевого происхождения, госпитализаций и смертей к продуктам питания с использованием данных о вспышках, США, 1998–2008 гг. Эмердж Инфекция Дис. 2013;19:407–15.
Артикул пабмед ПабМед Центральный Google Scholar
Berger CN, Sodha SV, Shaw RK, Griffin PM, Pink D, Hand P, Frankel G. Свежие фрукты и овощи как средства передачи патогенов человека. Окружающая среда микробиол. 2010;12(9):2385–97. https://doi.org/10.1111/j.1462-2920.2010.02297.
Артикул пабмед Google Scholar
Центры по контролю и профилактике заболеваний. Эпиднадзор за вспышками болезней пищевого происхождения — США, 2012 г.
 : годовой отчет. http://www.cdc.gov/foodsafety/fdoss/data/annual-summaries/index.html. По состоянию на 14 июня 2014 г.
: годовой отчет. http://www.cdc.gov/foodsafety/fdoss/data/annual-summaries/index.html. По состоянию на 14 июня 2014 г.Wendel AM, et al. Вспышка инфекции Escherichia coli O157:H7, связанная с употреблением в пищу упакованного шпината, в нескольких штатах, август – сентябрь 2006 г.: расследование в Висконсине. Клин Инфекция Дис. 2009;48:1079–86.
Артикул пабмед Google Scholar
Сориано Х.М., Рико Х., Молто Х.К., Маньес Х. Оценка микробиологического качества и обработка салата-латука, подаваемого в ресторанах университета. Int J Food Microbiol. 2000;58(1–2):123–8.
Артикул КАС пабмед Google Scholar
Amoah P, Drechsel P, Abaidoo RC, Klutse A. Эффективность обычных и усовершенствованных методов санитарной мойки в отдельных городах Западной Африки для снижения колиформных бактерий и яиц гельминтов на овощах.
 Троп Мед Int Health. 2007; 12 (Приложение 2): 40–50.
Троп Мед Int Health. 2007; 12 (Приложение 2): 40–50.Артикул пабмед Google Scholar
Mackey TJ, Carteney E. Практическая медицинская микробиология медицинской микробиологии, том. 2. 13-е изд. Лондон: Живой камень Черчилля; 1989. с. 204.
Google Scholar
Всемирная организация здравоохранения. Обеззараживание поверхности фруктов и овощей, употребляемых в пищу в сыром виде: обзор. 1998 г. http://www.who.int/foodsafety/publications/fs_management/surfac_decon/en/. По состоянию на 23 сентября 2010 г.
Эстрада-Гарсия Т., Лопес-Сауседо С., Замаррипа-Аяла Б. и др. Распространенность Escherichia coli и Salmonella spp. в уличной еде на открытых рынках (tianguis) и общей гигиенической и торговой практике в Мехико. Эпидемиол инфекции. 2004;132(6):1181–4.
Артикул КАС пабмед ПабМед Центральный Google Scholar
- «>
Ибрагим Т.А., Джуд-охей Б.С., Гива Э.О., Адеботе В.Т. микробиологический анализ и влияние выбранных антибактериальных средств на микробную нагрузку тыквы гофрированной, капусты и горьких листьев. Res J Agric Biol Sci. 2009;3(4):1143–5.
Google Scholar
Mritunjay SK, Kumar V. Потенциальная опасность микробного загрязнения, связанная с употреблением сырых салатных овощей и свежих продуктов. Ближний Восток J Sci Res. 2015; 23(4):741–9..
Google Scholar
Эрибо Б., Ашенафи М. Поведение Escherichia coli O157:H7 в томатах и переработанных томатных продуктах. Фуд Рез Инт. 2003; 36: 823–30.
Артикул Google Scholar
Майкл Дж.П., Чан ЭКС, Ноэль Р.К. Микробиология. 5-е изд. Нью-Дели: Тата Макгроу Хилл; 2005. с. 793–811.
Google Scholar
- «>
Камат А., Пингулкар К., Бхушан Б., Голап А., Томас П. Возможное применение низкодозового гамма-облучения для повышения микробиологической безопасности листьев свежего кориандра. Пищевой контроль. 2003;14(8):529–37.
Артикул Google Scholar
Ашрафи К., Валеро М.А., Массуд Дж. и др. Заражение человека растительным фасциолезом. Am J Trop Med Hyg. 2006;75(2):295–302.
ПабМед Google Scholar
Молинос А.С., Абриуэль Х., Бен Омар Н. и др. Влияние иммерсионных растворов, содержащих энтероцин AS-48, на Listeria monocytogenes в растительных продуктах. Appl Environ Microbiol. 2005;71(12):7781–7.
Артикул пабмед Google Scholar
Модельный формуляр ВОЗ 2008 г. (PDF). Всемирная организация здравоохранения. 2009. с. 295, 300. ISBN 9789241547659.
 Архивировано из оригинала 13 декабря 2016 г. http://apps.who.int/medicinedocs/en/d/Js16879.э/. По состоянию на 8 января 2017 г.
Архивировано из оригинала 13 декабря 2016 г. http://apps.who.int/medicinedocs/en/d/Js16879.э/. По состоянию на 8 января 2017 г.«19-й Примерный перечень основных лекарственных средств ВОЗ (апрель 2015 г.)». ВОЗ. Апрель 2015 г. https://www.scribd.com/document/356832183/19th-WHO-Model-List-of-Essential-Medicines-April-2015-pdf. По состоянию на 10 мая 2017 г.
Deichmann WB, Gerarde HW. Токсикология лекарств и химических веществ. Нью-Йорк: Академическая пресса; 1969.
Google Scholar
Скачать ссылки
Вклад авторов
Компания SHS задумала и разработала исследование, собрала образцы, обработала образец, проанализировала данные и написала рукопись. В.П. способствовал сбору и обработке образцов, а также анализу данных. IB способствовал написанию рукописи и критической оценке рукописи. NN и SG внесли свой вклад в уточнение результатов, обсуждение и подготовку рукописи. BS внес свой вклад в статистический анализ. Все авторы прочитали и одобрили окончательный вариант рукописи.
BS внес свой вклад в статистический анализ. Все авторы прочитали и одобрили окончательный вариант рукописи.
Благодарности
Авторы выражают благодарность преподавателям и техническому персоналу, кафедре микробиологии Манипальского университета, Индия и Манипальской учебной больнице, Непал, за техническую поддержку. Мы выражаем особую благодарность доктору Вандане К.Е., профессору микробиологии Медицинского колледжа Кастурба Манипальского университета, Индия, за незабываемую поддержку.
Конкурирующие интересы
Авторы заявляют об отсутствии конкурирующих интересов.
Наличие данных и материалов
Наборы данных, использованные и/или проанализированные в ходе текущего исследования, доступны у соответствующего автора по обоснованному запросу.
Согласие на публикацию
Не применимо.
Одобрение этики и согласие на участие
Предложение об исследовании было одобрено Институциональным комитетом по этике Медицинского колледжа Кастурба, Манипал, Индия.
Финансирование
Авторы не получали никакого финансирования от какого-либо агентства для поддержки работы, представленной в этой заявке.
Примечание издателя
Springer Nature остается нейтральной в отношении юрисдикционных претензий в опубликованных картах и институциональной принадлежности.
Информация об авторе
Авторы и организации
Манипальский колледж медицинских наук, Покхара, Непал
Супрам Хосуру Субраманья, Ниранджан Наяк, Шишир Гокхале и Бриджеш Сатьян 90 003
Медицинский колледж Малакки Манипала, Университет Манипала, Удупи, Индия
Васудха Пай и Индира Байри
- Супрам Хосуру Субраманья
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Vasudha Pai
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Indira Bairy
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Академия
- Ниранджан Наяк
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Shishir Gokhale
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Brijesh Sathian
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
Автор, ответственный за переписку
Супрам Хосуру Субраманья.
