Углекислый газ в атмосфере Земли — Википедия
 Изменения концентрации CO2 в ppm на протяжении последних 400 тыс. лет (сверху — за последнюю тысячу лет)
Изменения концентрации CO2 в ppm на протяжении последних 400 тыс. лет (сверху — за последнюю тысячу лет)Углеки́слый газ в атмосфе́ре Земли́ является компонентой с незначительной концентрацией в современной земной атмосфере, концентрация углекислого газа в сухом воздухе составляет 0,02—0,045 об. % (250—450 ppm). Углекислый газ составлял основу атмосферы молодой Земли наряду с азотом и водяным паром. Доля углекислого газа снижалась с момента появления океанов и зарождения жизни. Свободный кислород в атмосфере появился лишь 2 млрд лет назад. Начиная с середины XIX века отмечается устойчивый рост количества этого газа в атмосфере, с ноября 2015 года его среднемесячная концентрация стабильно превышает 400 ppm[1].
Роль углекислого газа (CO2, или диоксид углерода) в жизнедеятельности биосферы состоит прежде всего в поддержании фотосинтеза, который осуществляется растениями. Являясь парниковым газом, диоксид углерода в воздухе влияет на теплообмен планеты с окружающим пространством, эффективно блокируя переизлучаемое тепло на ряде частот, и таким образом участвует в формировании климата планеты
В связи с активным использованием человечеством ископаемых энергоносителей в качестве топлива происходит быстрое увеличение концентрации этого газа в атмосфере. Кроме того, по данным МГЭИК ООН, до 20 % антропогенных выбросов CO2 являются результатом обезлесения[3][4]. Впервые антропогенное влияние на концентрацию диоксида углерода отмечается с середины XIX века. Начиная с этого времени, темп его роста увеличивался и в конце 2000-х годов происходил со скоростью 2,20±0,01 ppm/год или 1,7 % за год. Согласно отдельным исследованиям, современный уровень CO2 в атмосфере является максимальным за последние 800 тыс. лет и, возможно, за последние 20 млн лет [5][6].
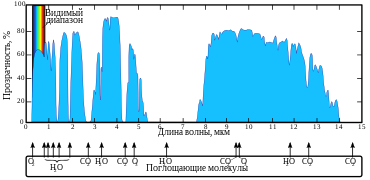 Спектр пропускания земной атмосферы (зависимость прозрачности от длины волны). Видны полосы поглощения CO2, O2, O3 и H2O.
Спектр пропускания земной атмосферы (зависимость прозрачности от длины волны). Видны полосы поглощения CO2, O2, O3 и H2O.Основным источником парникового эффекта в атмосфере Земли является водяной пар[7]. При отсутствии парниковых газов в атмосфере и значении солнечной постоянной, равной 1368 Вт⁄м2, средняя температура на поверхности должна составлять -19,5 °C. В действительности средняя температура поверхности Земли составляет +14 °C, то есть, парниковый эффект приводит к её увеличению на 34 °C[8]. При относительно небольшой концентрации в воздухе, CO2 является важной компонентой земной атмосферы, поскольку он поглощает и переизлучает инфракрасное излучение на различных длинах волн, включая длину волны 4,26 мкм (вибрационный режим — за счёт асимметричного растяжения молекулы) и 14,99 мкм (изгибные колебания молекулы). Данный процесс исключает или снижает излучение Земли в космос на этих длинах волн, что приводит к парниковому эффекту
Кроме инфракрасных свойств диоксида углерода, имеет значение тот факт, что он тяжелее воздуха. Так как средняя относительная молярная масса воздуха составляет 28,98 г/моль, а молярная масса CO2 — 44,01 г/моль, то увеличение доли углекислого газа приводит к увеличению плотности воздуха и, соответственно, к изменению профиля его давления в зависимости от высоты. В силу физической природы парникового эффекта, такое изменение свойств атмосферы приводит к увеличению средней температуры на поверхности[9]. Так как при увеличении доли этого газа в атмосфере его бо́льшая молярная масса приводит к росту плотности и давления, то при одной и той же температуре рост концентрации CO 2 приводит к увеличению влагоёмкости воздуха и к усилению парникового эффекта, обусловленного бо́льшим количеством воды в атмосфере[10][11][12]. Увеличение доли воды в воздухе для достижения одного и того же уровня относительной влажности — в силу малой молярной массы воды (18 г/моль) — снижает плотность воздуха, что компенсирует увеличение плотности, вызванное наличием повышенного уровня углекислого газа в атмосфере.
Комбинация перечисленных факторов в целом приводит к тому, что увеличение концентрации с доиндустриального уровня 280 ppm до современного 392 ppm (413,8 — 414 ppm на февраль 2020 [13] ) эквивалентно дополнительному выделению 1,8 Вт на каждый квадратный метр поверхности планеты[14]. Отличительной особенностью парниковых свойств диоксида углерода по сравнению с другими газами является его долговременное воздействие на климат, которое после прекращения вызвавшей его эмиссии остаётся в значительной степени постоянным на протяжении до тысячи лет. Другие парниковые газы, такие как метан и оксид азота, сохраняются в свободном состоянии в атмосфере не так долго
Теория глобального потепления не может объяснить тот факт, что содержание углекислого газа было когда то многократно выше (особенно до появления кислорода) но жизнь возникла и процветала, венерианский сценарий не реализовался. Это предполагает наличие отрицательной обратной связи. Таким «охлаждающим» эффектом могут служит облака, отражающие солнечную радиацию и возникающие при ещё большем содержании углекислого газа, чем есть сейчас. Оба явления, — потепления и похолодания, таким образом являются стабилизирующими механизмами для условий жизни на Земле. [18]

К естественным источникам диоксида углерода в атмосфере относятся вулканические извержения, сгорание органических веществ в воздухе и дыхание представителей животного мира (аэробные организмы). Также углекислый газ производится некоторыми микроорганизмами в результате процесса брожения, клеточного дыхания и в процессе гниения органических остатков в воздухе. К антропогенным источникам эмиссии CO2 в атмосферу относятся: сжигание ископаемых и неископаемых энергоносителей для получения тепла, производства электроэнергии, транспортировки людей и грузов. К значительному выделению CO2 приводят некоторые виды промышленной деятельности, такие, например, как производство цемента и утилизация попутных нефтяных газов путём их сжигания в факелах.
Растения преобразуют получаемый углекислый газ в углеводы в ходе фотосинтеза, который осуществляется посредством пигмента хлорофилла, использующего энергию солнечного излучения. Получаемый газ, кислород, высвобождается в атмосферу Земли и используется для дыхания гетеротрофными организмами и другими растениями, формируя таким образом цикл углерода.
Естественные источники[править | править код]
Большинство источников эмиссии по данным 98−го года РФ CO2 являются естественными. Перегнивание органического материала, такого как мёртвые деревья и трава, приводит к ежегодному выделению 220 млрд тонн диоксида углерода, земные океаны выделяют 330 млрд[14]. Пожары, возникающие в том числе по естественным причинам, из-за самого процесса горения в атмосфере и — в случае выгорания лесных массивов — за счет обезлесения приводят к эмиссии, которая сравнима с антропогенной. Например, в ходе индонезийских лесных и торфяных пожаров 1997 года (англ.)русск. было выделено 13—40 % от среднегодовой эмиссии CO2, получаемой в результате сжигания ископаемых топлив[19][20]. Вулканическая активность была главным источником углекислого газа во времена молодой Земли, в современный геологический период вулканическая эмиссия составляет около 130–230 млн тонн в год или менее 1 % от антропогенной [21][22].
В обычном состоянии эти естественные источники находятся в равновесии с физическими и биологическими процессами, удаляющими диоксид углерода из атмосферы — часть CO2 растворяется в морской воде и часть удаляется из воздуха в процессе фотосинтеза. Так как обычно в ходе данного процесса поглощается 5,5⋅1011 т диоксида углерода в год, а его общая масса в земной атмосфере составляет 3,03 ⋅1012 т, то в среднем весь атмосферный CO2 участвует в углеродном цикле раз в шесть лет[14]. Из-за наличия антропогенных выбросов поглощение CO2биосферой превосходило его выделение на ≈17 млрд тонн в середине 2000-х годов, скорость его поглощения имеет устойчивую тенденцию к увеличению вместе с ростом атмосферной концентрации
Антропогенная эмиссия[править | править код]
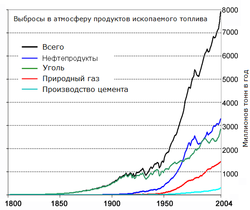 Эмиссия углекислого газа в атмосферу в результате промышленной деятельности в 1800—2004 гг.
Эмиссия углекислого газа в атмосферу в результате промышленной деятельности в 1800—2004 гг.С наступлением промышленной революции в середине XIX века происходило поступательное увеличение антропогенных выбросов диоксида углерода в атмосферу, что привело к нарушению баланса углеродного цикла и росту концентрации CO2. В настоящее время около 57 % производимого человечеством углекислого газа удаляется из атмосферы растениями и океанами[24]. Соотношение увеличения количества CO2 в атмосфере ко всему выделенному CO2 составляет постоянную величину порядка 45 % и претерпевает короткопериодические колебания и колебания с периодом в пять лет[23].
Сжигание ископаемых топлив, — таких как уголь, нефть и природный газ, является основной причиной эмиссии антропогенного CO 2. Вырубка лесов является второй по значимости причиной. В 2008 году в результате сжигания ископаемого топлива в атмосферу было выделено 8,67 млрд тонн углерода (31,8 млрд тонн CO2), в то время как в 1990 году годовая эмиссия углерода составляла 6,14 млрд тонн[25]. Сводка лесов под землепользование привела к увеличению содержания атмосферного диоксида углерода, эквивалентное сжиганию 1,2 млрд тонн угля в 2008 году (1,64 млрд тонн в 1990)[25]. Суммарное увеличение за 18 лет составляет 3 % от ежегодного естественного цикла CO2, что достаточно для выведения системы из равновесия и для ускоренного роста уровня CO2[26]. Как результат, диоксид углерода постепенно аккумулируется в атмосфере, и в 2009 году его концентрация на 39 % превысила доиндустриальное значение[27].
Таким образом, несмотря на то, что (по состоянию на 2011 год) суммарное антропогенное выделение CO
Изменение температуры и углеродный цикл[править | править код]
К другим факторам, увеличивающим содержание CO2 в атмосфере, следует отнести рост средней температуры в XX веке, что должно было отражаться в ускорении перегнивания органических остатков и, в силу прогрева океанов, в снижении общего количества диоксида углерода, растворяемого в воде. Увеличение температуры происходило в том числе по причине исключительно высокой солнечной активности в этот период и в XIX веке (см., например, событие Кэррингтона, 1859 г.)[28].
При переходе от условий холодного к теплому климату в течение последнего миллиона лет, естественное изменение концентрации атмосферного CO2 оставалось в пределах 100 ppm, то есть суммарное увеличение его содержания не превосходило 40 %[29]. При этом, например, средняя температура планеты в период климатического оптимума 9000—5000 лет до н. э. была приблизительно на 1—2 °C выше современной, а из-за более сильно выраженного парникового эффекта в условиях тёплого климата среднегодовая аномалия температуры в субарктических широтах достигала 9 °C[30].
Влияние вулканизма[править | править код]

Современный вулканизм в среднем приводит к выделению 2⋅108 тонн CO2 в год, что составляет величину менее 1 % от антропогенной эмиссии[21]. Основное отличие этого вида эмиссии от антропогенной состоит в том, что при сжигании ископаемых энергоносителей в воздухе происходит замещение молекул кислорода молекулами углекислого газа, то есть суммарное увеличение массы атмосферы соответствует массе сожжённого углерода, тогда как при вулканических извержениях происходит увеличение массы атмосферы на величину, равную массе выделенного газа.
Углекислый газ — второй по количеству (после водяного пара) газ, выделяемый вулканами. Большинство газа, выделяемого подводными вулканами, оказывается растворённым в воде[31]. Изотопный состав выделяемого диоксида углерода примерно соответствует изотопному составу атмосферного CO2, получаемого в результате сжигания ископаемых энергоносителей, что затрудняет точное определение объёма вулканической эмиссии CO2[31].
Крупные вулканические извержения могут приводить к значительному выделению диоксида углерода в атмосферу, но такие извержения происходят редко — несколько событий за столетие — и в среднем не оказывают заметного влияния на уровень эмиссии этого газа в атмосферу. Например, при извержении вулкана Лаки 1783 года выделилось примерно 90 млн тонн CO2, при извержении Тамбора в 1815 году около 48 млн тонн[31]. Отдельные исследования указывают на несколько бо́льшее выделение диоксида углерода при упомянутых выше извержениях (Лаки 1783 г, ≈6,5⋅108 т), но относительная редкость подобных событий делает их влияние на содержание углекислого газа несущественным и в этом случае[31].
Последним извержением категории VEI 6 было извержение вулкана Пинатубо 1991 года. Его основное воздействие на содержание углекислого газа в атмосфере состояло в выделении аэрозолей в стратосферу и, как следствие, в нарушении баланса углеродного цикла из-за снижения на 0,5 °C средней температуры на планете по причине антипарникового эффекта. Увеличение амплитуды сезонных колебаний на графике Килинга в этот период времени указывает на некоторое улучшение условий для осуществления фотосинтеза растениями в начале 1990-х годов. Последнее объясняется эффектом рассеяния солнечного излучения на частицах стратосферного аэрозоля, что и привело к увеличению потребления атмосферного CO2 растительностью[32].
Современная концентрация углекислого газа в атмосфере[править | править код]
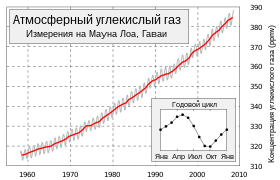
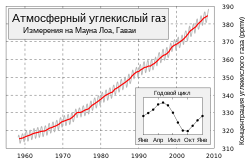 Изменение концентрации CO2 за 50 лет.
Изменение концентрации CO2 за 50 лет.В современный период времени концентрация углекислого газа сохраняет устойчивый рост, в 2009 году средняя концентрация CO2 в земной атмосфере составляла 0,0387 % или 387 ppm, в сентябре 2016 года превысила 400 ppm[33][34].
Вместе с годовым ростом 2,20±0,01 ppm, в течение года наблюдается периодическое изменение концентрации амплитудой 3—9 ppm, которое следует за развитием вегетационного периода в Северном полушарии. Потому как в северной части планеты располагаются все основные континенты, влияние растительности Северного полушария доминирует в годовом цикле концентрации CO2. Уровень достигает максимума в мае и минимума в октябре, когда количество биомассы, осуществляющей фотосинтез, является наибольшим[35].
Весной 2016 года австралийские ученые установили, что концентрация диоксида углерода в атмосфере в районе острова Тасмания достигла 400 ppm[36].
В 2017 году Всемирная метеорологическая организация сообщила, что концентрация диоксида углерода в атмосфере Земли достигла самого высокого уровня за последние 800 тысяч лет уровня: 403,3 ppm[37].
В апреле 2018 года по данным Погодной обсерватории на Мауна-Лоа, средняя концентрация CO2 достигла значения 410,26 ppm (или 0,041026 % углекислого газа в воздухе)[38]. На апрель 2018 года, такой среднемесячный показатель наблюдался впервые за всю историю человеческой цивилизации[39].
11 мая 2019 года, зафиксирован новый рекорд концентрации CO2 в атмосфере: 415,28 ppm (или 0,041528 % углекислого газа в воздухе)[40][41].
Наиболее достоверным способом измерения концентраций атмосферного диоксида углерода в период времени до начала прямых измерений является определение его количества в пузырьках воздуха, заключенных в ледяных кернах из материковых ледников Антарктиды и Гренландии. Наиболее широко в этих целях используются антарктические керны, согласно которым уровень атмосферного CO2 оставался в пределах 260—284 ppm до начала промышленной революции в середине XIX века и на протяжении 10 тыс. лет до этого момента времени[42]. Отдельные исследования, основанные на изучении ископаемой листвы, указывают на гораздо более существенные изменения уровня CO2 в этот период (~300 ppm), но они подвергаются критике[43][44]. Также керны, взятые в Гренландии, указывают на бо́льшую степень изменения концентрации углекислого газа по сравнению с результатами, полученными в Антарктиде. Но при этом исследователи гренландских кернов предполагают, что бо́льшая вариативность здесь обусловлена локальными осадками карбоната кальция[45]. В случае низкого уровня пыли в образцах льда, взятого в Гренландии, данные по уровням CO2 в течение голоцена хорошо согласуются с данными из Антарктики.
Наиболее продолжительный период измерений уровней CO2 на основании изучения ледяных кернов возможен в Восточной Антарктиде, где возраст льда достигает 800 тыс. лет, и который показывает, что концентрация диоксида углерода изменялась в пределах 180—210 ppm во время ледниковых периодов и увеличивалась до 280—300 ppm в более теплые периоды[5][29][46].
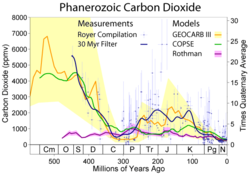 Изменения концентрации атмосферного углекислого газа в течение фанерозоя (последние 541 млн лет, современность справа). В течение бо́льшей части последних 550 млн лет уровень CO2 значительно превосходил современный.
Изменения концентрации атмосферного углекислого газа в течение фанерозоя (последние 541 млн лет, современность справа). В течение бо́льшей части последних 550 млн лет уровень CO2 значительно превосходил современный.На более продолжительных интервалах времени содержание атмосферного CO2 определяется на основании определения баланса геохимических процессов, включая определение количества материала органического происхождения в осадочных породах, выветривание силикатных пород и вулканизм в изучаемый период. На протяжении десятков миллионов лет в случае любого нарушения равновесия в цикле углерода происходило последующее уменьшение концентрации CO2. Потому как скорость этих процессов исключительно низка, установка взаимосвязи эмиссии диоксида углерода с последующим изменением его уровня в течение следующих сотен лет является сложной задачей.
Для изучения концентрации углекислого газа в прошлом также используются различные косвенные (англ.)русск. методы датирования. Они включают определение соотношения изотопов бора и углерода в некоторых типах морских осадочных пород и количество устьиц в ископаемой листве растений. Несмотря на то, что эти измерения менее точны, чем данные по ледяным кернам, они позволяют определить очень высокие концентрации CO2 в прошлом, которые 150—200 млн лет назад составляли 3 000 ppm (0,3 %) и 400—600 млн лет назад — 6 000 ppm (0,6 %)[6].
Снижение уровня атмосферного CO2 прекратилось в начале пермского периода, но продолжилось, начиная примерно с 60 млн лет назад. На рубеже эоцена и олигоцена (34 миллиона лет назад — начало формирования современного ледяного щита Антарктиды) количество CO2 составляло 760 ppm[47]. По геохимическим данным было установлено, что уровень углекислого газа в атмосфере достиг доиндустриального уровня 20 млн лет назад и составлял 300 ppm.
Взаимосвязь с концентрацией в океане[править | править код]
 Обмен диоксидом углерода между водоёмами и воздухом
Обмен диоксидом углерода между водоёмами и воздухомВ земных океанах диоксида углерода в сто раз больше, чем в атмосфере — 36⋅1012 тонн в пересчёте на углерод. Растворенный в воде CO2 содержится в виде гидрокарбонат- и карбонат-ионов. Гидрокарбонаты получаются в результате реакций между скальными породами, водой и CO2. Одним из примеров является разложение карбоната кальция:
- CaCO3+CO2+h3O⟷Ca2+ + 2HCO3−{\displaystyle {\ce {CaCO3 + CO2 + h3O <-> Ca^{2+}\ +\ 2HCO3-}}}.
Реакции, подобные этой, приводят к сглаживанию колебаний концентрации атмосферного CO2. Так как правая часть реакции содержит кислоту, добавление CO2 в левой части уменьшает pH, то есть приводит к закислению океана. Другие реакции между диоксидом углерода и некарбонатными породами тоже приводят к образованию угольной кислоты и его ионов.
Данный процесс обратим, что приводит к образованию известняковых и других карбонатных пород с высвобождением половины гидрокарбонатов в виде CO2. В течение сотен миллионов лет этот процесс привёл к связыванию в карбонатных породах бо́льшей части первоначального диоксида углерода из протоатмосферы Земли. В конечном итоге большинство CO2, полученного в результате антропогенной эмиссии, будет растворено в океане, но скорость, с которой будет происходить этот процесс в будущем, остается не до конца определённой[48].
Влияние концентрации CO2 в атмосфере на продуктивность растений (фотосинтеза)[править | править код]
По способу фиксации CO2 подавляющее большинство растений относятся к типам фотосинтеза С3 и С4. К группе С3 принадлежит большинство известных видов растений (около 95% растительной биомассы Земли это С3-растения). К группе С4 принадлежат некоторые травянистые растения, в том числе важные сельскохозяйственные культуры: кукуруза, сахарный тростник, просо.
С4-механизм фиксации углерода выработался как приспособление к условиям низких концентраций CO2 в атмосфере. Практически у всех видов растений рост концентрации CO2 в воздухе приводит к активизации фотосинтеза и ускорению роста.
У С3-растений кривая начинает выходить на плато при концентрации CO2 более 1000 ppm.
Однако у С4-растений рост скорости фотосинтеза прекращается уже при концентрации CO2 в 400 ppm. Поэтому современная его концентрация, составляющая на данный момент более 400 молекул на миллион (ppm), уже достигла оптимума для фотосинтеза у С4-растений, но всё еще очень далека от оптимума для С3-растений.
По экспериментальным данным, удвоение текущей концентрации CO2 приведет (в среднем) к ускорению прироста биомассы у С3-растений на 41 %, а у С4 — на 22 %.
Добавление в окружающий воздух 300 ppm CO2 приведет к росту продуктивности у С3-растений на 49 % и у С4 — на 20 %, у фруктовых деревьев и бахчевых культур — на 24 %, бобовых — на 44 %, корнеплодных — на 48 %, овощных — на 37 %.
С 1971 по 1990 г., на фоне роста концентрации CO2 на 9 %, отмечалось увеличение содержания биомассы в лесах Европы на 25–30 %[49].
- ↑ Mauna Loa CO2 monthly mean data (англ.). Earth System Research Laboratory. Дата обращения 16 мая 2018.
- ↑ 1 2 (англ.) Petty, G. W.: A First Course in Atmospheric Radiation, pages 229—251, Sundog Publishing, 2004
- ↑ http://www.ipcc.ch/pdf/assessment-report/ar4/wg1/ar4-wg1-chapter7.pdf IPCC Fourth Assessment Report, Working Group I Report «The Physical Science Basis», Section 7.3.1.2 (p. 514-515)
- ↑ www.un.org: Изменение климата.
- ↑ 1 2 (англ.) Deep ice tells long climate story, BBC News (4 сентября 2006). Дата обращения 28 апреля 2010.
- ↑ 1 2 (англ.) Climate Change 2001: The Scientific Basis Архивная копия от 27 апреля 2007 на Wayback Machine
- ↑ Подрезов А. О., Аламанов С. К.; Лелевкин В. М., Подрезов О. А., Балбакова Ф. Изменение климата и водные проблемы в Центральной Азии. Учебный курс для студентов естественных и гуманитарных специальностей. Москва – Бишкек, 2006 (неопр.) (недоступная ссылка) 18. Дата обращения 16 июня 2012. Архивировано 12 июля 2012 года.
- ↑ Calculating Planetary Energy Balance & Temperature | UCAR Center for Science Education (неопр.). scied.ucar.edu. Дата обращения 29 июня 2019.
- ↑ ПРИРОДА ПАРНИКОВОГО ЭФФЕКТА Архивная копия от 1 мая 2009 на Wayback Machine, Объединенный Научный Совет РАН по проблемам Геоинформатики
- ↑ (англ.) An Introduction to Air Density and Density Altitude Calculations, 1998 — 2012 Richard Shelquist
- ↑ Абсолютная и относительная влажность
- ↑ (англ.) Humidity 101 Архивировано 16 апреля 2013 года., World Water Rescue Foundation
- ↑ Концентрация со2 в воздухе, данные за последнюю неделю (рус.). The World Only. Дата обращения 10 февраля 2020.
- ↑ 1 2 3 4 Изменение климата, торговля углеродом и биоразнообразие, World Bank Group: Хабиба Гитай
- ↑ (англ.) Irreversible climate change due to carbon dioxide emissions — PNAS
- ↑ (англ.) WMO statement on the globa climate in 2010 Архивная копия от 11 мая 2011 на Wayback Machine
- ↑ (англ.) Bundle Up, It’s Global Warming, JUDAH COHEN, 25.12.2010
- ↑ (англ.) Impact of decadal cloud variations on the Earth’s energy budget
- ↑ (англ.) Indonesian Wildfires Accelerated Global Warming
- ↑ (англ.) Massive peat burn is speeding climate change — 06 November 2004 — New Scientist
- ↑ 1 2 (англ.) Gerlach, T. M., 1992, Present-day CO2 emissions from volcanoes: Eos, Transactions, American Geophysical Union, Vol. 72, No. 23, June 4, 1991, pp. 249, and 254–255
- ↑ (англ.) U.S. Geological Survey, «Volcanic Gases and Their Effects», volcanoes.usgs.gov
- ↑ 1 2 Keeling et al., 1995
- ↑ (англ.) Abstract, Contributions to accelerating atmospheric CO2 growth from economic activity, carbon intensity, and efficiency of natural sinks.
- ↑ 1 2 (англ.) Global carbon budget 2008 Архивная копия от 12 января 2016 на Wayback Machine, lgmacweb.env.uea.ac.uk Архивная копия от 5 марта 2016 на Wayback Machine
- ↑ (англ.) US Global Change Research Information Office, «Common Questions about Climate Change»
- ↑ (англ.) Carbon Budget 2009 Highlights Архивная копия от 16 декабря 2011 на Wayback Machine, The Global Carbon Project.
- ↑ (англ.) Usoskin, Ilya G.; Usoskin, Ilya G.; Solanki, Sami K. (англ.)русск.; Schüssler, Manfred; Mursula, Kalevi; Alanko, Katja. A Millennium Scale Sunspot Number Reconstruction: Evidence For an Unusually Active Sun Since the 1940’s (англ.) // Physical Review Letters : journal. — 2003. — Vol. 91. — P. 211101. — doi:10.1103/PhysRevLett.91.211101.
- ↑ 1 2 (англ.) Vostok Ice Core Data, ncdc.noaa.gov
- ↑ (англ.) V.L. Koshkarova and A.D. Koshkarov. Regional signatures of changing landscape and climate of northern central Siberia in the Holocene (англ.) // Russian Geology and Geophysics : journal. — 2004. — Vol. 45, no. 6. — P. 672—685.
- ↑ 1 2 3 4 (англ.) Volcanic Carbon Dioxide, Timothy Casey
- ↑ (англ.) Mount Pinatubo as a Test of Climate Feedback Mechanisms, Alan Robock, Department of Environmental Sciences, Rutgers University
- ↑ (англ.) Tans, Pieter. Globally averaged marine surface monthly mean data (неопр.). NOAA/ESRL. Дата обращения 19 февраля 2014.
- ↑ (англ.) Current atmospheric CO2 concentration at http://co2unting.com (неопр.) (недоступная ссылка). Дата обращения 21 июня 2019. Архивировано 12 июля 2012 года.
- ↑ (англ.) Carbon Dioxide Information Analysis Center (CDIAC) — Frequently Asked Questions
- ↑ ТАСС: Наука — Австралийские ученые: уровень углекислого газа в мировой атмосфере достиг точки невозврата
- ↑ Концентрация CO2 в атмосфере выросла до максимума за 800 тыс. лет (неопр.) (недоступная ссылка). Дата обращения 30 октября 2017. Архивировано 7 ноября 2017 года.
- ↑ Mooney C. Earth’s atmosphere just crossed another troubling climate change threshold // The Washington Post. 2018-05-03.
- ↑ Farand C. dioxide levels in Earth’s atmosphere reach ‘highest level in 800,000 years // The Independent. 2018-05-05.
- ↑ CO2 in the atmosphere just exceeded 415 parts per million for the first time in human history (англ.). TechCrunch. Дата обращения 1 августа 2019.
- ↑ Animation of Keeling Curve History Updated to Include 2019 Milestone (англ.). The Keeling Curve (4 June 2019). Дата обращения 1 августа 2019.
- ↑ (англ.) Historical CO2 record derived from a spline fit (20 year cutoff) of the Law Dome DE08 and DE08-2 ice cores (неопр.). Дата обращения 12 июня 2007. Архивировано 12 июля 2012 года.
- ↑ (англ.) Wagner, Friederike; Bent Aaby and Henk Visscher. Rapid atmospheric O2 changes associated with the 8,200-years-B.P. cooling event (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 2002. — Vol. 99, no. 19. — P. 12011—12014. — doi:10.1073/pnas.182420699. — PMID 12202744.
- ↑ (англ.) Indermühle, Andreas; Bernhard Stauffer, Thomas F. Stocker. Early Holocene Atmospheric CO2 Concentrations (англ.) // Science : journal. — 1999. — Vol. 286, no. 5446. — P. 1815. — doi:10.1126/science.286.5446.1815a.
- ↑ (англ.) Smith, H. J.; M Wahlen and D. Mastroianni. The CO2 concentration of air trapped in GISP2 ice from the Last Glacial Maximum-Holocene transition (англ.) // Geophysical Research Letters (англ.)русск. : journal. — 1997. — Vol. 24, no. 1. — P. 1 — 4. — doi:10.1029/96GL03700.
- ↑ (англ.) Chemical & Engineering News: Latest News — Ice Core Record Extended
- ↑ (англ.) New CO2 data helps unlock the secrets of Antarctic formation September 13th, 2009
- ↑ (англ.) Archer, D. (2005). Fate of fossil fuel CO2 in geologic time. J. Geophys. Res., 110.
- ↑ Реакция растений на рост концентрации углекислого газа в атмосфере, Акатов П. В.
Диоксид углерода — Википедия
| Диоксид углерода | |||
|---|---|---|---|
| |||
({{{изображение}}}) | |||
| Систематическое наименование | Диоксид углерода | ||
| Традиционные названия | углекислый газ, углекислота, двуокись углерода, сухой лёд (в твёрдом состоянии) | ||
| Хим. формула | CO2 | ||
| Рац. формула | CO2 | ||
| Состояние | бесцветный газ | ||
| Молярная масса | 44,01 г/моль | ||
| Плотность | газ (0 °C): 1,9768 кг/м³ жидкость (0 °С, 35,5 ат): 925 кг/м³ тв. (−78,5 °C): 1560 кг/м³ | ||
| Динамическая вязкость | 8,5⋅10−5 Па·с (10°C, 5,7 МПа) | ||
| Энергия ионизации | 13,77 ± 0,01 эВ[3] | ||
| Скорость звука в веществе | 269 м/с | ||
| Температура | |||
| • сублимации | −78,5 °C | ||
| Тройная точка | −56,6 °C, 0,52 МПа [1] | ||
| Критическая точка | 31 °C, 7,38 МПа | ||
| Критическая плотность | 467 кг/м³ см³/моль | ||
| Уд. теплоёмк. | 849 Дж/(кг·К) | ||
| Теплопроводность | 0,0166 Вт/(м·K) | ||
| Энтальпия | |||
| • образования | 394 кДж/моль | ||
| • плавления | 9,02 кДж/моль | ||
| • кипения | 16,7 кДж/моль | ||
| • сублимации | 26 кДж/моль | ||
| Удельная теплота испарения | 379,5 кДж/кг | ||
| Удельная теплота плавления | 205 кДж/кг | ||
| Давление пара | 56,5 ± 0,1 атм[3] | ||
| Растворимость | |||
| • в воде | 1,48 кг/м³ | ||
| Рег. номер CAS | 124-38-9 | ||
| PubChem | 280 | ||
| Рег. номер EINECS | 204-696-9 | ||
| SMILES | |||
| InChI | |||
| Кодекс Алиментариус | E290 | ||
| RTECS | FF6400000 | ||
| ChEBI | 16526 | ||
| Номер ООН | 1013 | ||
| ChemSpider | 274 | ||
| Предельная концентрация | 9 г/м³ (5 000 ppm) долговременное воздействие, 54 г/м³ (30 000 ppm) кратковременное воздействие (<15 мин) [2] | ||
| ЛД50 | LC50: 90 000 [источник?] мг/м3*5 мин (человек, ингаляция) | ||
| Токсичность | Нетоксичен. Опасен лишь в очень больших количествах (обладает удушающим действием). Негорюч. | ||
| Фразы безопасности (S) | S9, S23, S36 | ||
| NFPA 704 |  | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
 Медиафайлы на Викискладе Медиафайлы на Викискладе | |||
Диокси́д углеро́да или двуо́кись углеро́да (также углеки́слый газ, углекислотá, окси́д углеро́да(IV), у́гольный ангидри́д) — бесцветный газ (в нормальных условиях), почти без запаха (в больших концентрациях с кисловатым «содовым» запахом), с химической формулой CO2.
Плотность при нормальных условиях 1,98 кг/м³ (в 1,5 раза тяжелее воздуха). При атмосферном давлении диоксид углерода не существует в жидком состоянии, переходя непосредственно из твёрдого состояния в газообразное (возгонка). Твёрдый диоксид углерода называют сухим льдом. При повышенном давлении и обычных температурах углекислый газ переходит в жидкость, что используется для его хранения.
Концентрация углекислого газа в атмосфере Земли составляет в среднем 0,04 %[4]. Углекислый газ легко пропускает излучение в ультрафиолетовой и видимой частях спектра, которое поступает на Землю от Солнца и обогревает её. В то же время он поглощает испускаемое Землёй инфракрасное излучение и является одним из парниковых газов, вследствие чего должен участвовать в процессе глобального потепления[уточнить]. Изначально, до появления жизни, углекислый газ составлял основу атмосферы Земли и его уровень снижался от десятков процентов до долей одного в результате процесса фотосинтеза. Постоянный рост уровня содержания этого газа в атмосфере наблюдается с начала индустриальной эпохи[источник не указан 199 дней]. Рост содержания углекислого газа выше, до определённой концентрации, приводит к появлению облаков из углекислоты, что ведет к похолоданию.[5] Оба эти явления объясняют, почему температурные условия существования жизни на Земле относительно стабильны в течение миллиардов лет.
Физические[править | править код]
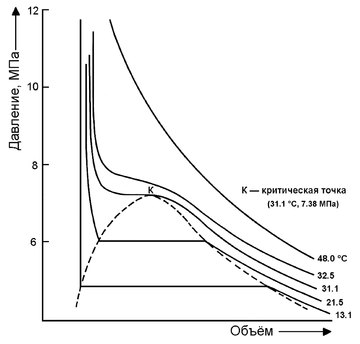
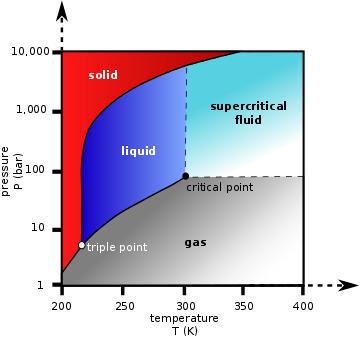 Фазовая диаграмма диоксида углерода
Фазовая диаграмма диоксида углеродаОксид углерода (IV) (углекислый газ) — бесцветный газ, при малых концентрациях в воздухе не имеет запаха, при больших концентрациях имеет характерный кисловатый запах газированной воды. Тяжелее воздуха приблизительно в 1,5 раза.
Молекула углекислого газа линейна, расстояние от центра центрального атома углерода до центров двух атомов кислорода 116,3 пм.
При температуре −78,3 °С кристаллизуется в виде белой снегообразной массы — «сухого льда». Сухой лёд при атмосферном давлении не плавится, а испаряется, не переходя в жидкое состояние, температура сублимации −78 °С. Жидкий углекислый газ можно получить при повышении давления. Так, при температуре 20 °С и давлении свыше 6 МПа (~60 атм) газ сгущается в бесцветную жидкость. В спокойном электрическом разряде светится характерным бело-зелёным светом.
Негорюч, но в его атмосфере может поддерживаться горение активных металлов, например, щелочных металлов и щелочноземельных — магния, кальция, бария.
Углекислый газ образуется при гниении и горении органических веществ. Содержится в воздухе и минеральных источниках, выделяется при дыхании животных и растений. Растворим в воде (0,738 объёмов углекислого газа в одном объёме воды при 15 °С).
Химические[править | править код]
По химическим свойствам диоксид углерода относится к кислотным оксидам. При растворении в воде образует нестойкую угольную кислоту. Реагирует со щёлочами с образованием её солей — карбонатов и гидрокарбонатов. Вступает в реакции электрофильного замещения (например, с фенолом) и нуклеофильного присоединения (например, с магнийорганическими соединениями).
Оксид углерода(IV) останавливает горение, вытесняя кислород из зоны реакции. В нём горят только некоторые активные металлы[6]:
- 2Mg+CO2⟶2MgO+C{\displaystyle {\ce {2Mg + CO2 -> 2MgO + C}}}.
Взаимодействие с оксидом активного металла:
- CaO+CO2⟶CaCO3{\displaystyle {\ce {CaO + CO2 -> CaCO3}}}.
При растворении в воде образует равновесную смесь раствора диоксида углерода и угольной кислоты, причём равновесие сильно сдвинуто в сторону разложения кислоты:
- CO2↑+h3O⇄h3CO3{\displaystyle {\ce {CO2\uparrow +h3O\rightleftarrows h3CO3}}}.
Реагирует со щёлочами с образованием карбонатов и гидрокарбонатов:
- Ca(OH)2+CO2⟶CaCO3↓+h3O{\displaystyle {\ce {Ca(OH)2 + CO2 -> CaCO3 v + h3O}}} (качественная реакция на углекислый газ),
- KOH+CO2⟶KHCO3{\displaystyle {\ce {KOH + CO2 -> KHCO3}}}.
Биологические[править | править код]
Организм человека выделяет приблизительно 1 кг углекислого газа в сутки.[7]
Этот углекислый газ переносится от тканей, где он образуется в качестве одного из конечных продуктов метаболизма, по венозной системе и затем выделяется с выдыхаемым воздухом через лёгкие. Таким образом, содержание углекислого газа в крови велико в венозной системе, уменьшается в капиллярной сети лёгких, и мало в артериальной крови. Содержание углекислого газа в пробе крови часто выражают в терминах парциального давления, то есть давления, которое бы имел содержащийся в пробе крови в данном количестве углекислый газ, если бы весь объём пробы крови занимал только он[8].
Содержание углекислого газа в крови человека приблизительно таково:
Референтные значения или средние значения парциального давления углекислого газа в крови (pCO2) Единицы измерения Газ венозной крови Альвеолярный лёгочный газ Газ артериальной крови кПа 5,5[9]—6,8[9] 4,8 4,7[9]—6,0[9] мм рт. ст. 41—51 36 35[10]—45[10]
Углекислый газ транспортируется в крови тремя различными способами (точное соотношение каждого из этих трёх способов транспортировки зависит от того, является ли кровь артериальной или венозной).
- Бо́льшая часть углекислого газа (от 70 % до 80 %) преобразуется ферментом карбоангидразой эритроцитов в ионы гидрокарбоната[11] при помощи реакции CO2+h3O⟶h3CO3⟶H++HCO3−{\displaystyle {\ce {CO2 + h3O -> h3CO3 -> H^+ + HCO3^-}}}.
- Около 5—10 % углекислого газа растворено в плазме крови[11].
- Около 5—10 % углекислого газа связано с гемоглобином в виде карбаминосоединений (карбогемоглобин)[11].
Гемоглобин, основной кислород-транспортирующий белок эритроцитов крови, способен транспортировать как кислород, так и углекислый газ. Однако углекислый газ связывается с гемоглобином в ином месте, чем кислород. Он связывается с N-терминальными концами цепей глобина, а не с гемом. Однако благодаря аллостерическим эффектам, которые приводят к изменению конфигурации молекулы гемоглобина при связывании, связывание углекислого газа понижает способность кислорода к связыванию с ним же, при данном парциальном давлении кислорода, и наоборот — связывание кислорода с гемоглобином понижает способность углекислого газа к связыванию с ним же, при данном парциальном давлении углекислого газа. Помимо этого, способность гемоглобина к преимущественному связыванию с кислородом или с углекислым газом зависит также и от pH среды. Эти особенности очень важны для успешного захвата и транспорта кислорода из лёгких в ткани и его успешного высвобождения в тканях, а также для успешного захвата и транспорта углекислого газа из тканей в лёгкие и его высвобождения там.
Углекислый газ является одним из важнейших медиаторов ауторегуляции кровотока. Он является мощным вазодилататором. Соответственно, если уровень углекислого газа в ткани или в крови повышается (например, вследствие интенсивного метаболизма — вызванного, скажем, физической нагрузкой, воспалением, повреждением тканей, или вследствие затруднения кровотока, ишемии ткани), то капилляры расширяются, что приводит к увеличению кровотока и соответственно к увеличению доставки к тканям кислорода и транспорта из тканей накопившейся углекислоты. Кроме того, углекислый газ в определённых концентрациях (повышенных, но ещё не достигающих токсических значений) оказывает положительное инотропное и хронотропное действие на миокард и повышает его чувствительность к адреналину, что приводит к увеличению силы и частоты сердечных сокращений, величины сердечного выброса и, как следствие, ударного и минутного объёма крови. Это также способствует коррекции тканевой гипоксии и гиперкапнии (повышенного уровня углекислоты).
Ионы гидрокарбоната очень важны для регуляции pH крови и поддержания нормального кислотно-щелочного равновесия. Частота дыхания влияет на содержание углекислого газа в крови. Слабое или замедленное дыхание вызывает респираторный ацидоз, в то время как учащённое и чрезмерно глубокое дыхание приводит к гипервентиляции и развитию респираторного алкалоза.
Кроме того, углекислый газ также важен в регуляции дыхания. Хотя наш организм требует кислорода для обеспечения метаболизма, низкое содержание кислорода в крови или в тканях обычно не стимулирует дыхание (вернее, стимулирующее влияние нехватки кислорода на дыхание слишком слабо и «включается» поздно, при очень низких уровнях кислорода в крови, при которых человек нередко уже теряет сознание). В норме дыхание стимулируется повышением уровня углекислого газа в крови. Дыхательный центр гораздо более чувствителен к повышению уровня углекислого газа, чем к нехватке кислорода. Как следствие этого, дыхание сильно разрежённым воздухом (с низким парциальным давлением кислорода) или газовой смесью, вообще не содержащей кислорода (например, 100 % азотом или 100 % закисью азота) может быстро привести к потере сознания без возникновения ощущения нехватки воздуха (поскольку уровень углекислоты в крови не повышается, ибо ничто не препятствует её выдыханию). Это особенно опасно для пилотов военных самолётов, летающих на больших высотах (в случае аварийной разгерметизации кабины пилоты могут быстро потерять сознание). Эта особенность системы регуляции дыхания также является причиной того, почему в самолётах стюардессы инструктируют пассажиров в случае разгерметизации салона самолёта в первую очередь надевать кислородную маску самим, прежде чем пытаться помочь кому-либо ещё — делая это, помогающий рискует быстро потерять сознание сам, причём даже не ощущая до последнего момента какого-либо дискомфорта и потребности в кислороде[11].
Дыхательный центр человека пытается поддерживать парциальное давление углекислого газа в артериальной крови не выше 50 мм ртутного столба. При сознательной гипервентиляции содержание углекислого газа в артериальной крови может снизиться до 10—20 мм ртутного столба, при этом содержание кислорода в крови практически не изменится или увеличится незначительно, а потребность сделать очередной вдох уменьшится как следствие уменьшения стимулирующего влияния углекислого газа на активность дыхательного центра. Это является причиной того, почему после некоторого периода сознательной гипервентиляции легче задержать дыхание надолго, чем без предшествующей гипервентиляции. Такая сознательная гипервентиляция с последующей задержкой дыхания может привести к потере сознания до того, как человек ощутит потребность сделать вдох. В безопасной обстановке такая потеря сознания ничем особенным не грозит (потеряв сознание, человек потеряет и контроль над собой, перестанет задерживать дыхание и сделает вдох, дыхание, а вместе с ним и снабжение мозга кислородом восстановятся, а затем восстановится и сознание). Однако в других ситуациях, например, перед нырянием, это может быть опасным (потеря сознания и потребность сделать вдох наступят на глубине, и в отсутствие сознательного контроля в дыхательные пути попадёт вода, что может привести к утоплению)[источник не указан 894 дня]. Именно поэтому гипервентиляция перед нырянием опасна и не рекомендуется.
- В промышленных количествах углекислота выделяется из дымовых газов, или как побочный продукт химических процессов, например, при разложении природных карбонатов[12] (известняк, доломит) или при производстве алкоголя (спиртовое брожение). Смесь полученных газов промывают раствором карбоната калия, которые поглощают углекислый газ, переходя в гидрокарбонат. Раствор гидрокарбоната при нагревании или при пониженном давлении разлагается, высвобождая углекислоту. В современных установках получения углекислого газа вместо гидрокарбоната чаще применяется водный раствор моноэтаноламина, который при определённых условиях способен абсорбировать CO2{\displaystyle {\ce {CO2}}}, содержащийся в дымовом газе, а при нагреве отдавать его; таким образом отделяется готовый продукт от других веществ.
- Также углекислый газ получают на установках разделения воздуха как побочный продукт получения чистого кислорода, азота и аргона.
В лабораторных условиях небольшие количества получают взаимодействием карбонатов и гидрокарбонатов с кислотами, например мрамора, мела или соды с соляной кислотой, используя, например, аппарат Киппа[12].
- CaCO3+2HCl⟶CaCl2+h3O+CO2↑{\displaystyle {\ce {CaCO3 + 2HCl -> CaCl2 + h3O + CO2 ^}}}.
Использование реакции серной кислоты с мелом или мрамором приводит к образованию малорастворимого сульфата кальция, который замедляет реакцию, и который удаляется значительным избытком кислоты с образованием кислого сульфата кальция.
Для приготовления сухих напитков может быть использована реакция пищевой соды с лимонной кислотой или с кислым лимонным соком. Именно в таком виде появились первые газированные напитки. Их изготовлением и продажей занимались аптекари.
Также для получения углекислого газа применяется зкзотермическая реакция горения углерода в кислороде[12]:
- C+O2⟶CO2↑+394kJ{\displaystyle {\ce {C + O2 -> CO2 ^ + 394 kJ}}}.
В пищевой промышленности углекислота используется как консервант и разрыхлитель, обозначается на упаковке кодом Е290.
В криохирургии используется как одно из основных веществ для криоабляции новообразований.
Жидкая углекислота широко применяется в системах пожаротушения и в огнетушителях. Автоматические углекислотные установки для пожаротушения различаются по системам пуска, которые бывают пневматическими, механическими или электрическими.
Устройство для подачи углекислого газа в аквариум может включать в себя резервуар с газом. Простейший и наиболее распространённый метод получения углекислого газа основан на конструкции для изготовления алкогольного напитка браги. При брожении выделяемый углекислый газ вполне может обеспечить подкормку аквариумных растений[13].
Углекислый газ используется для газирования лимонада, газированной воды и других напитков. Углекислый газ используется также в качестве защитной среды при сварке проволокой, но при высоких температурах происходит его распад с выделением кислорода. Выделяющийся кислород окисляет металл. В связи с этим приходится в сварочную проволоку вводить раскислители, такие как марганец и кремний. Другим следствием влияния кислорода, также связанного с окислением, является резкое снижение поверхностного натяжения, что приводит, среди прочего, к более интенсивному разбрызгиванию металла, чем при сварке в инертной среде.
Углекислота в баллончиках применяется в пневматическом оружии (в газобаллонной пневматике) и в качестве источника энергии для двигателей в авиамоделировании.
Хранение углекислоты в стальном баллоне в сжиженном состоянии выгоднее, чем в виде газа. Углекислота имеет сравнительно низкую критическую температуру +31 °С. В стандартный 40-литровый баллон заливают около 20 кг сжиженного углекислого газа, и при комнатной температуре в баллоне будет находиться жидкая фаза, а давление составит примерно 6 МПа (60 кгс/см²). Если температура будет выше +31 °С, то углекислота перейдёт в сверхкритическое состояние с давлением выше 7,36 МПа. Стандартное рабочее давление для обычного 40-литрового баллона составляет 15 МПа (150 кгс/см²), однако он должен безопасно выдерживать давление в 1,5 раза выше, то есть 22,5 МПа, — таким образом, работа с подобными баллонами может считаться вполне безопасной.
Твёрдая углекислота — «сухой лёд» — используется в качестве хладагента в лабораторных исследованиях, в розничной торговле, при ремонте оборудования (например: охлаждение одной из сопрягаемых деталей при их посадке внатяжку) и так далее. Для сжижения углекислого газа и получения сухого льда применяются углекислотные установки.
Измерение парциального давления углекислого газа требуется в технологических процессах, в медицинских применениях — анализ дыхательных смесей при искусственной вентиляции лёгких и в замкнутых системах жизнеобеспечения. Анализ концентрации CO₂ в атмосфере используется для экологических и научных исследований, для изучения парникового эффекта. Углекислый газ регистрируют с помощью газоанализаторов основанных на принципе инфракрасной спектроскопии и других газоизмерительных систем. Медицинский газоанализатор для регистрации содержания углекислоты в выдыхаемом воздухе называется капнограф. Для измерения низких концентраций CO₂ (а также CO) в технологических газах или в атмосферном воздухе можно использовать газохроматографический метод с метанатором и регистрацией на пламенно-ионизационном детекторе[14].
Ежегодные колебания концентрации атмосферной углекислоты на планете определяются, главным образом, растительностью средних (40—70°) широт Северного полушария.
Вегетация в тропиках практически не зависит от сезона, сухой пояс пустынь 20—30° (обоих полушарий) даёт малый вклад в круговорот углекислоты, а полосы суши, наиболее покрытые растительностью, расположены на Земле асимметрично (в Южном полушарии в средних широтах находится океан).
Поэтому с марта по сентябрь вследствие фотосинтеза содержание СО2 в атмосфере падает, а с октября по февраль — повышается. Вклад в зимний прирост дают как окисление древесины (гетеротрофное дыхание растений, гниение, разложение гумуса, лесные пожары), так и сжигание ископаемого топлива (угля, нефти, газа), заметно увеличивающееся в зимний сезон[15].
Большое количество углекислоты растворено в океане.
Углекислый газ составляет значительную часть атмосфер некоторых планет Солнечной системы: Венеры, Марса.
Углекислый газ в высоких концентрациях токсичен[16]; при вдыхании его повышенных концентраций в воздухе по воздействию на воздуходышащие живые организмы его относят к удушающим газам (англ.)русск.. По ГОСТу (ГОСТ 8050-85) углекислота относится к IV классу опасности.
Незначительные повышения концентрации, вплоть до 0,2−0,4 % (2000−4000 ppm), в помещениях приводят к развитию у людей сонливости и слабости. Опасными для здоровья концентрациями считаются концентрации около 7−10 %, при которых развиваются симптомы удушья, проявляющиеся в виде головной боли, головокружения, расстройстве слуха и в потере сознания (симптомы, сходные с симптомами высотной болезни), эти симптомы развиваются, в зависимости от концентрации, в течение времени от нескольких минут до одного часа.
Для помещений нормальным является уровень CO₂ около 600 ppm (частей на миллион). Повышенные концентрации углекислого газа снижают когнитивные способности людей. Уже при 1200 ppm расширяются кровеносные сосуды в мозге, снижается активность нейронов и уменьшается объём коммуникации между регионами мозга.[17]. В школьных классах типичной является концентрация 2000−2500, а общий разброс значений — от 1000 до 6000, это вызывает обеспокоенность у исследователей[18], поскольку выявлено снижение результатов учеников, выполняющих тестовые задания в душных помещениях[19].
| Влияние на взрослых здоровых людей | Концентрация углекислого газа, ppm |
|---|---|
| Нормальный уровень на открытом воздухе | 350—450 |
| Приемлемые уровни | <600 |
| Жалобы на несвежий воздух | 600—1000 |
| Максимальный уровень стандартов ASHRAE и OSHA[20] | 1000 |
| Общая вялость | 1000—2500 |
| Возможны нежелательные эффекты на здоровье | 1000—2500 |
| Максимально допустимая концентрация в течение 8 часового рабочего дня | 5000 |
При вдыхании воздуха с очень высокими концентрациями газа смерть наступает очень быстро от удушья, вызванного гипоксией[21]. Такой случай произошёл 28 февраля 2020 года когда в одном из банных комплексов Москвы в бассейн было высыпано 30 кг сухого льда который при возгонке вытеснил над водой воздух к потолку, в результате чего погибло 3 человека[22].
Несмотря на то, что даже концентрация 5—7 % CO₂ в воздухе несмертельна, но при концентрации 0,1 % (такое содержание углекислого газа иногда наблюдается в воздухе мегаполисов), люди начинают чувствовать слабость, сонливость. Это показывает, что даже при высоком уровне кислорода, большая концентрация CO₂ существенно влияет на самочувствие человека.
| Симптомы у взрослых здоровых людей[23] | Концентрация углекислого газа, ppm |
|---|---|
| Легкое отравление, учащается пульс и частота дыхания, тошнота и рвота | 30 000 |
| Добавляется головная боль и легкое нарушение сознания | 50 000 |
| Потеря сознания, в дальнейшем — смерть | 100 000 |
Вдыхание воздуха с повышенной концентрацией этого газа не приводит к долговременным расстройствам здоровья. После удаления пострадавшего из атмосферы с высокой концентрацией углекислого газа быстро наступает полное восстановление здоровья и самочувствия[24].
- ↑ Carbon Dioxide — Thermophysical Properties
- ↑ Carbon dioxide: Immediately Dangerous to Life or Health Concentrations (IDLH)
- ↑ 1 2 http://www.cdc.gov/niosh/npg/npgd0103.html
- ↑ Trends in Atmospheric Carbon Dioxide (англ.). National Oceanic and Atmospheric Administration. Дата обращения 24 сентября 2013.
- ↑ Chen Zhou, Mark D. Zelinka & Stephen A. Klein. Impact of decadal cloud variations on the Earth’s energy budget (англ.). Nature Geoscience. Дата обращения 4 декабря 2019.
- ↑ А. С. Егоров. Репетитор по химии — Ростов-на-Дону: «Феникс», 2009.
- ↑ 7. How much carbon dioxide do humans contribute through breathing?. Frequent Questions — Emissions (англ.). US EPA. Дата обращения 4 декабря 2019. Архивировано 2 февраля 2011 года.
- ↑ Charles Henrickson. Chemistry (неопр.). — Cliffs Notes, 2005. — ISBN 0-7645-7419-1.
- ↑ 1 2 3 4 Пересчитано из значений в мм. рт. ст. с использованием коэффициента пересчёта 0,133322 кПа/мм. рт. ст.
- ↑ 1 2 Таблица референсных значений. Юго-Западный медицинский центр при Университете Далласа.
- ↑ 1 2 3 4 Carbon dioxide (неопр.). solarnavigator.net. Дата обращения 12 октября 2007.
- ↑ 1 2 3 Glinka, Nikolaj Leonidovič (1882-1965). Obŝaâ himiâ. — Izd. 27-e ster. — Leningrad: «Himiâ», 1988. — 702, [2] s. с. — ISBN 5724500035, 9785724500036.
- ↑ Большая Энциклопедия Нефти и Газа.
- ↑ ГОСТ 31371.6-2008 (ИСО 6974-6:2002). Газ природный. Определение состава методом газовой хроматографии с оценкой неопределённости. Часть 6. Определение водорода, гелия, кислорода, азота, диоксида углерода и углеводородов C1 — C8 с использованием трёх капиллярных колонок (рус.). Docs.cntd.ru. — М.: Стандартинформ, 2009.. Дата обращения 4 декабря 2019.
- ↑ Бялко А. В. Растения убыстряют рост // Природа. — 1996. — № 10. (по Keeling C.D., Whorf Т.P., Wahlen M., van der Plicht J. // Nature. 1995. V. 375, № 6533. P.666-670)
- ↑ https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5380556/
- ↑ Greenwood, Veronique. Is Conference Room Air Making You Dumber? : [англ.] // The New York Times : газ. — 2019. — 6 May.
- ↑ Ventilation rates and carbon dioxide concentrations in schools. — In: Ventilation with Outdoor Air : [англ.] // Berkeley Lab : [сайт]. — 2019.
- ↑ Сорокин, Андрей. «Глобальное потепление отупляет. От этого уже страдают школьники и офисные работники» // Republic : [сайт]. — 2020. — 7 января.
- ↑ Indoor Air Quality in Commercial and Institutional Buildings
- ↑ (англ.) Carbon Dioxide as a Fire Suppressant: Examining the Risks, U.S. Environmental Protection Agency:.
- ↑ Производитель сухого льда высказался о его токсичности после гибели россиян.
- ↑ Приемлемые и опасные уровни концентрации углекислого газа (CO2) согласно ASHRAE и OSHA — США. Рекомендованные уровни вентиляции помещений.
- ↑ (англ.) Glatte Jr H. A., Motsay G. J., Welch B. E. Carbon Dioxide Tolerance Studies (неопр.) // Brooks AFB, TX School of Aerospace Medicine Technical Report. — 1967. — Т. SAM—TR—67—77.
- Вукалович М. П., Алтунин В. В. Теплофизические свойства двуокиси углерода. — М.: Атомиздат, 1965. — 456 с.
- Тезиков А. Д. Производство и применение сухого льда. — М.: Госторгиздат, 1960. — 128 с.
- Гродник М. Г., Величанский А. Я. Проектирование и эксплуатация углекислотных установок. — М.: Пищевая промышленность, 1966. — 275 с.
- Талянкер Ю. Е. Особенности хранения баллонов со сжиженным газом //
Охота на душный воздух, часть 1. Сколько СО2 в Москве? / Tion corporate blog / Habr
Открываем цикл статей о том, чем дышат жители разных городов. Начали со столицы. Генеральный директор «Тион Умный микроклимат» Михаил Амелькин проехался по Москве с датчиком СО2 и лично проверил столичный воздух.Почему СО2?
Подавляющее большинство специалистов в области вентиляции сходятся во мнении: углекислый газ является индикатором состояния воздуха (авторитетный пруф из АВОК). Много СО2 — значит, много и более вредных веществ (формальдегиды и прочая ядовитая органика, PM2.5 и т.д.). Это логично: ведь если вентиляция не справляется с воздухообменом, то в помещении накапливается и выдыхаемый нами СО2, и весь остальной «воздушный коктейль». Так что вполне резонно измерять концентрацию СО2 в воздухе, чтобы оценить качество этого самого воздуха.
Является ли углекислый газ таким же загрязнителем воздуха, как автомобильные выхлопы или промышленные выбросы? Исследования на эту тему противоречивы. Есть много статей про вред СО2 (пример раз, пример два). Меньше исследований, согласно которым углекислый газ практически безвреден, но и такие есть (пример). Если вам интересна эта тема, пишите в комментариях. В будущем мы можем сделать подробный литобзор о влиянии СО2 на здоровье человека.
Наше мнение — углекислый газ однозначно влияет на самочувствие человека (вялость, утомляемость, сонливость). Вспомните, как вы чувствуете себя в душном офисе или квартире с закрытыми окнами. Усредненное влияние СО2 на человека выглядит примерно так:
Как измерить количество СО2 в воздухе?
Уровень углекислого газа в воздухе измеряется в ppm: 1 ppm = 0.0001%, то есть одна миллионная доля. Для России 1400 ppm углекислого газа в воздухе — это уже недопустимое количество (согласно ГОСТу 30494—2011). В Америке общие стандарты ASHRAE (американское общество инженеров по отоплению, охлаждению и кондиционированию воздуха) гласят: жалобы на головную боль начинаются с 2000 ppm.
В среднем по больнице получается такая картина:
- 300 ppm – норма на улице на природе
- 500 ppm – норма на улице в современном городе
- 700-1500 ppm – норма в помещении, причем ближе к 1500 ppm уже начинаются жалобы на духоту, головную боль, вялость и т.д.
Последнее из вступительной части — название использованного датчика СО2. Это был Testo 480.
Все, заканчиваем с введением. Приступаем непосредственно к измерением. Слово Михаилу Амелькину.
Транспорт
Трип начался с самолёта. Перелет Новосибирск-Москва, около 4 часов. Самолёт полный, аэробус А316. Весь полёт концентрация СО2 около 2000 ppm! Добавьте сюда слишком высокую температуру на борту (около 28°С) и пониженное давление (786 гПа против 1007 гПа на земле), и поймете, почему нас так «колбасит» после перелетов. Для сравнения, в аэропорту прилета около 700 ppm, то есть норма. На обратном пути летел в полупустом самолёте и ситуация была гораздо лучше – весь полёт до 1000 ppm, что приемлемо.
Далее был аэроэкспресс. Оказалось, что при полном вагоне вентиляция тоже не справляется – более 1800 ppm! А вот на пути обратно вагон был пустой и вентиляция справлялась – около 500 ppm.
В метро все гораздо лучше. На самой станции под землёй 600 ppm. В старых, «дырявых» вагонах около 700 ppm. Вот в новых вагонах метро, где кондиционеры гоняют воздух по кругу, уже хуже – при неполной загрузке 1200 ppm. В набитом вагоне следует ожидать больше 2000 ppm. Но здесь стоит иметь в виду, что обычно в таких вагонах мы проводим мало времени, 10-20 минут, так что это не очень критично.
Улица
Сделал замер прямо на Красной Площади. Уровень около 450 ppm. Это выше, чем за городом, что, скорее всего, объясняется обилием транспорта, котельных и промышленности, которые активно выделяют в воздух СО2, создавая над городом «пузырь» углекислого газа. Но это не страшно. Пока.
Дом и отель
Мне повезло, и в моём номере всю ночь концентрация СО2 была меньше 600 ppm. Отлично! Я спал не в духоте. Это потому, что попросил номер с окном во двор и смог держать окно на микропроветривании, не просыпаясь от шума машин. Но вентиляции в номере нет, поэтому плата за свежий воздух тоже не малая — московский смог. Была бы вентиляшка с профессиональными фильтрами — было бы на пятерочку!
Надо сказать, что замеры в квартирах с закрытыми окнами часто показывают очень плохие результаты, пара человек в комнате запросто могут «надышать» 2000 ppm минут за 40-60. А окна обычно закрыты, чтобы не было сквозняков и шума с улицы. Вывод тот же, что и в случае с отелем – дома вентиляция must have. При этом проще и дешевле поставить компактные бризеры, чем заморачиваться с полноценной вентиляцией.
Рестораны и кинотеатры
Тут картина сильно разная, но одно очевидно (кто-то скажет, что это ясно и без приборов) – любят наши рестораторы экономить на вентиляшке! Например, у меня была деловая встреча в кофейне «Хлеб насущный» на Никольской. Место хорошее, но вот с воздухом беда – 2000 ppm! В такой атмосфере очень сложно думать и решать деловые вопросы. В «Чайхоне №1» на Пушкинской было чуть лучше, до 1500 ppm.
Но есть и хорошие места: в «Старбакс» на Площади революции и в «Пять звёзд» на Павелецкой 700 ppm и 800 ppm соответственно. А вот в самом кинозале этого замечательного кинотеатра было «не айс» — до 1500 ppm весь сеанс. При этом администрация не поскупилась на кондиционеры – в залах было прохладно и это «скрашивало» ситуацию. Но кондеи не заменяют вентиляцию! Температура – температурой, а кислород – кислородом, должно быть и то, и другое.
Пока это вся информация по Москве. Обязуюсь сделать обзорный трип в Новосибирске. Что можно сказать по итогу?
Выводы
По полученным данным однозначно можно констатировать низкое качество воздуха в транспорте, особенно когда в нем много пассажиров. Пара советов, что делать в душном самолёте.
- Используйте обдув, он есть в каждом самолёте на потолке или «в спинке впереди стоящего кресла». Оттуда воздух идет тоже с превышением по СО2 (проверено), но он хотя бы раздувает тот «пузырь» углекислого газа, который вы вокруг себя «надышали».
- Если в салоне жарко, раздевайтесь. Пусть будет чуть прохладно. Чем ниже температура тела, тем лучше кровь насыщается кислородом и выводится углекислота.
- Сведите активность к минимуму. Лучше спать или «медитировать». Постарайтесь не нервничать, не брать в уме тройные интегралы. Помните, мозг потребляет около 20% всего кислорода в крови!
- Если курите, лучше не курить за несколько часов до полёта. Это позволит очистить кровь от угарного газа и улучшит снабжение мозга кислородом. Лучше используйте никотиновые жвачки/таблетки/пластыри.
- После прилета проведите часок на улице, продышитесь, сделайте дыхательную гимнастику, нормализуйте биохимию в крови. Дайте мозгу прийти в себя!
Что касается мест отдыха, то там самое коварство — в кондиционерах. Опыт показывает, что в прохладном воздухе создается ощущение комфорта, в то время как уровень СО2 достигает критических значений. Интерьер, комфорт, «атмосфера» есть, а настоящей здоровой атмосферы может не быть. Далеко не во всех заведениях состояние воздуха бывает удовлетворительным. Воздух не видно – значит, на нём можно сэкономить. Если бы все посетители имели портативные датчики и регулярно жаловались на превышение уровня СО2, возможно, тогда владельцы заведений внимательнее относились бы к вопросам вентиляции.
В этот раз не получилось «поохотиться» на СО2 в школах, детсадах и офисах, но есть основания считать, что и там регулярно наблюдаются превышенные концентрации углекислого газа. Немного заспойлерю: уже сделали замеры СО2 в классе одной из новосибирских школ – больше 2000 ppm! А дети же там должны учиться и работать головой. А как требовать от ребенка концентрации и успеваемости, когда голова не варит просто физиологически?
Примечание Tion: скоро будет материал про наше мини-исследование в школе.
Короче, я хочу выбирать места работы и отдыха еще и по качеству воздуха. Верю, что это существенно улучшит «среднюю температуру по палате» — самочувствие моё и моей семьи.
Михаил Амелькин
Концентрация углекислого газа в атмосфере Земли достигла исторического максимума — Общество
НЬЮ-ЙОРК, 13 мая. /ТАСС/. Концентрация углекислого газа (CO2) в земной атмосфере впервые в истории человечества превысила 415 частей на миллион (ppm) — то есть в каждом куб. м воздуха присутствует не менее 415 мл углекислого газа. Об этом сообщила в понедельник телекомпания CNN.
По ее данным, рекордный показатель — 415,26 ppm — был зафиксирован в субботу специалистами обсерватории Национального управления США по исследованию океанов и атмосферы (NOAA), расположенной у вершины вулкана Мауна-Лоа на острове Гавайи.
«Это впервые в истории человечества <…> Не только в задокументированной истории, не с момента появления сельского хозяйства 10 тыс. лет назад», — отметил американский метеоролог Эрик Холтхаус.
Как указала CNN, до этого больше всего CO2 в атмосфере Земли было около 3 млн лет назад — в эпоху плиоцена. Тогда, по предположениям ученых, его концентрация составляла от 310 до 400 ppm. Согласно данным Института океанографии Скриппса при Калифорнийском университете в Сан-Диего, в течение 800 тыс. лет до индустриальной революции содержание СО2 в атмосфере никогда не превышало 300 ppm. Уровень 400 ppm впервые в истории был отмечен в 2013 году.
Повышение концентрации CO2 в атмосфере способствует возникновению парникового эффекта. Подавляющее число экспертов считает, что деятельность человека, который сжигает ископаемое топливо, — одна из основных причин потепления климата на Земле.
В целях борьбы с глобальным потеплением в 2015 году по итогам 21-й конференции Рамочной конвенции об изменении климата, состоявшейся в Париже, было принято Парижское соглашение по климату. 197 участников форума условились не допустить повышения средней температуры на планете к 2100 году более чем на 2 градуса по Цельсию в сравнении с доиндустриальной эпохой. Ученые полагают, что более значительный рост температуры может привести к необратимым последствиям для экологии. Парижское соглашение должно прийти на смену Киотскому протоколу, срок действия которого истечет в 2020 году.
Уровень CO2 в атмосфере достиг невиданной в истории отметки. Что это означает для планеты и здоровья людей — Мир
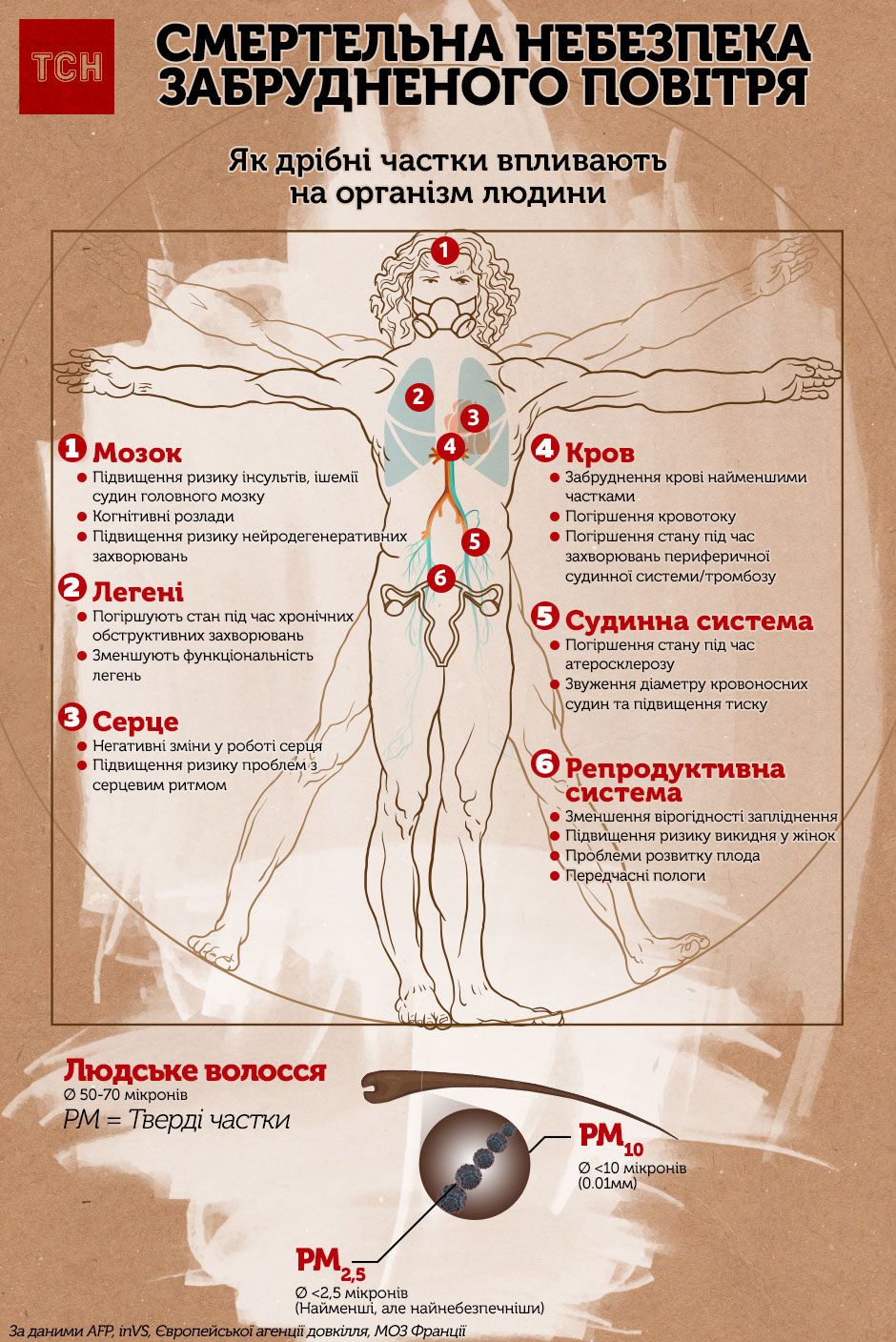
Загрязненный воздух не только вызывает глобальное потепление, но и провоцирует различные заболевания у людей.
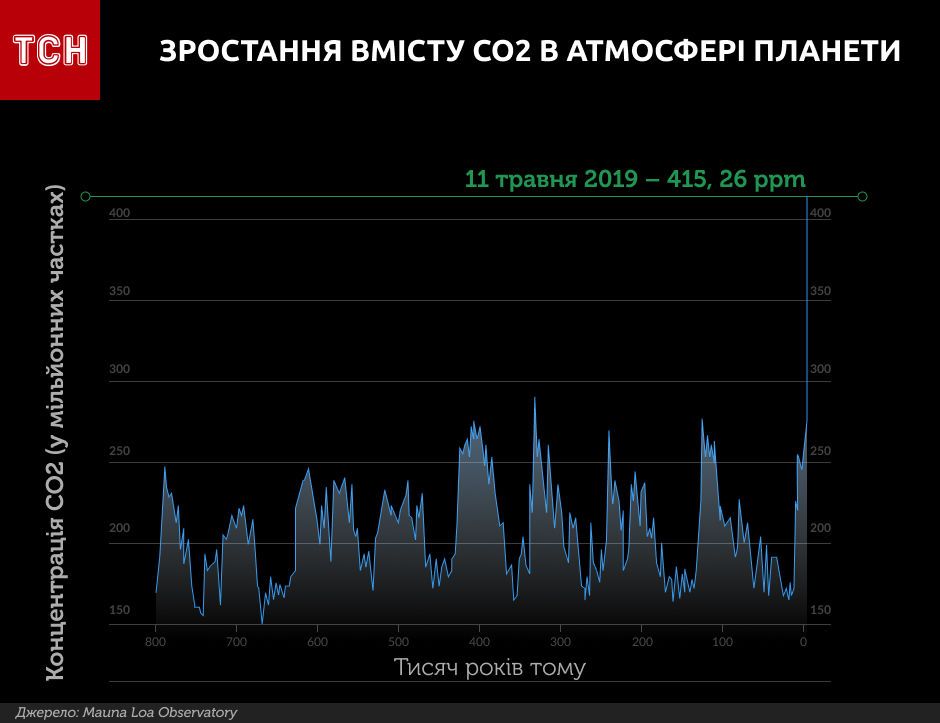
Концентрация углекислого газа в атмосфере планеты впервые за последние 800 тысяч лет превысила отметку 415 миллионных частиц. Такое загрязнение является неслыханным.
Об этом свидетельствуют данные наблюдений океанографического института Скриппс (Scripps Institution), который ежедневно измеряет уровень углекислого газа на горе Мауна Лоа совместно с учеными из Национального управления по вопросам океана и атмосферы.
Непрерывные измерения количества углекислого газа на горе начались в 1958 году. Тогда концентрация CO2 не превышала 333 ppm (миллионных долей).
Ситуация, что сложилась сейчас, является беспрецедентной. «Это первый случай, когда в атмосфере нашей планеты было зафиксировано свыше 415 ppm CO2. Такого не было, когда 10 тысяч лет было изобретено сельское хозяйство. Такого не было, когда миллионы лет назад появились современные люди», — прокомментировал находку метеоролог Эрик Голтгаус в посте в Twitter.
Увеличение уровня загрязнения
Измерения количества углекислого газа в воздухе на горе Мауна Лоа в 1958 году начал Девин Килин. В честь ученого позже было названо и графу Киллинга – график, описывающий изменения концентрации углекислого газа в воздухе.
Согласно результатам исследований, с марта 1958 года по ноябрь 2018-го количество углекислого газа в воздухе возросло с 333 до 406 ppm. В среднем за год количество СО2 увеличивалось примерно на 2 ppm.
Читайте также:
На Эвересте находят тела давно погибших альпинистов. Рассказываем, какое отношение к этому имеет глобальное потепление
Наибольший «прирост» пришелся на двадцатый век. Если в 1910 году содержание CO2 в атмосфере насчитывало 300 ppm, что уже выше, чем за последние 800 тысяч лет, то за последние сто лет оно увеличилось более чем на 100 миллионных частиц карбон диоксида.
Причиной роста стало увеличение сжигания ископаемых пород и вырубка значительных массивов лесов (в частности, для расширения сельскохозяйственных угодий и городских участков). Вследствие этого естественный цикл охлаждения претерпел изменений – тепло стало скапливаться у поверхности.
 tsn.ua
tsn.uaЭто нанесло значительный ущерб экологии планеты – высвобождение в атмосферу CO2 и других парниковых газов уже привело к росту глобальных температур на 1 градус по Цельсию.
В прошлом году ученые предупредили, что если тенденция продолжится, то глобальное потепление в конечном итоге приведет к ряду катаклизмов и составит прямую угрозу как для жизни человека, так и миллионов других организмов, населяющих планету.
Активно поступают в атмосферу планеты и окислы азота, которые также способствуют «парниковому эффекту». Они выделяются в результате любого из ископаемых видов топлива, содержащих азотные соединения.
Угрозу представляют также и фреоны – эти соединения выделяются в результате деятельности человека (в частности, вследствие функционирования холодильников и морозильников). Они повышают уровень ультрафиолетового облучения Земли из космоса и также способствуют парниковому эффекту.
Влияние на здоровье
Однако рост количества соединений-загрязнителей воздуха и влечет угрозу не только экологии, но и здоровью людей. К примеру, в результате неполного сгорания полезных ископаемых выделяется также монооксид углерода СО – токсичный газ, который губительно влияет на сердечно-сосудистую систему человека.
Его вредный для экологии родственник – CO2 – для здоровья вреден только в больших количествах и может вызвать головокружение, тошноту и другие симптомы нехватки кислорода.
Читайте также:
Миллионам животных и растений угрожает вымирание, люди тоже в опасности. Объясняем, почему
Зато такие соединения как ртуть и свинец приводят к отравлению органов и могут вызвать повреждение мозга и даже смерть.
По данным Всемирной организации здравоохранения, загрязненный воздух ежегодно убивает 7 миллионов человек. А по статистике, девять из 10 людей дышат им в опасном для здоровья количестве.
СпецпроектиГлобальное потепление. Как Земля меняет свое лицо
Одна треть от всех смертей от рака легких или сердечно-сосудистых заболеваний случается из-за того, что люди дышали загрязненным воздухом. А около 14% детей в возрасте от 5 до 18 лет страдают из-за него астмой. Ежегодно от вызванных загрязненным воздухом респираторных заболеваний погибают 543 тысячи детей младше 5 лет.
Как отмечается в ВОЗ, грязный воздух повышает риск того, что ребенок при рождении будет иметь низкий вес или родится преждевременно. Вдыхание матерью загрязненного воздуха может привести также к задержке развития мозга зародыша.
Читайте также:
Земля значительно позеленела за последние 20 лет. Рассказываем, как это произошло и при чем здесь Китай
Существуют также доказательства того, что он также способен негативно повлиять на здоровье людей, которые болеют диабетом.
Однако негативное влияние загрязненного воздуха не ограничивается физическим здоровьем людей. Он наносит вред также моральному здоровью.
Влияние на когнитивные способности и психику
Ряд исследований доказал, что у людей, которые дышат исполненным химическими соединениями воздухом, возрастает риск проблем с психикой. Они также чаще получают плохие оценки в школе и даже с большей вероятностью прибегают к преступлениям.
Так, в 2011 году Сефи Рот, ученый из Лондонской школы экономики, решил узнать, как именно загрязненный воздух влияет на когнитивные способности.
Он анализировал результаты, полученные учениками одинакового уровня образования за экзамен в разные дни. Место проведения экзамена не менялось. Ежедневно ученые измеряли загрязнения воздуха в регионе – позже они сопоставили его с результатами детей.
Выяснилось, что дети, которые сдавали экзамен тогда, когда воздух был грязнеее, получали худшие оценки, чем их сверстники. Это впоследствии сказалось и на их будущем – они вступили в худшие университеты и зарабатывали значительно меньше даже через 10 лет после эксперимента.
«Поэтому даже когда эффект от загрязнения воздуха является кратковременным, он все равно может иметь долгосрочные последствия», – подчеркнул Рот.
В 2018 году ученый провел еще одно исследование, в рамках которого анализировал влияние загрязненного воздуха на уголовные преступления – в дни, когда загрязнение было большим, количество мелких преступлений как в богатых, так и в бедных районах города возрастало.
 ТСН.ua
ТСН.uaА еще одно исследование, проведенное Джексоном Лу, подтвердило, что явление может влиять и на куда более серьезные преступления. Ученые в течение девяти лет собирали данные из более 9 тысяч городов в США и пришли к выводу, что загрязнение воздуха увеличивает вероятность шести категорий преступлений – убийств, изнасилований, ограблений, угонов автомобилей и сексуального насилия.
Возможной причиной феномена ухудшения человеческого поведения на фоне загрязнения является то, что некоторые химические элементы способны повредить структуру мозга и связи между нейронами.
«Дело может быть в том, что определенные загрязнители воздуха повреждают передлобную долю мозга», – отмечает исследовательница из университета Южной Калифорнии Диана Юнан. Ведь именно этот участок отвечает за человеческие импульсы, исполнительные функции организма и самоконтроль.
Читайте также:
Гренландия начала стремительно таять. Означает ли это, что человечеству грозит всемирный потоп
Влияет загрязнение воздуха также и на психическое здоровье людей. Так, исследование, опубликованное в марте 2019 года, установило, что подростки, которые дышат токсичным и загрязненным воздухом, чаще страдают паранойей и слышат голоса.
Ведущая автор исследования Джоан Ньюбеси из Королевского колледжа Лондона отмечает, что стопроцентно о причинно-следственные связи между этими явлениями говорить рано. Однако результаты подтверждают выводы других работ относительно того, что загрязнение воздуха действительно может вызывать проблемы с психикой.
Видео У человечества есть 12 лет, чтобы остановить глобальное потепление — ученые ООН
12 лет до мировой катастрофы. Именно столько имеет человечество, чтобы остановить глобальное потепление, считают ученые из ООН, занимающиеся вопросами климата. Действовать ученые призывают немедленно, ведь уже к 2030 году уровень выбросов углекислого газа в атмосферу может достичь критической отметки. А повышение температуры будет иметь необратимые последствия: привычным явлением могут стать лесные пожары, засуха, жара, ураганы, наводнения — а затем неурожай.

замеры уровня CO2 в различных местах и ситуациях / Комфортная жизнь / iXBT Live
На улице, в общественном транспорте, офисе, однушке, включая кухню, и в салоне автомобиля с закрытой заслонкой. В последнем случае шанс умереть отнюдь не призрачный, а вполне реальный, и его можно легко вычислить.

В чем проблема
Вдыхаем кислород, выдыхаем углекислый газ. В выдохе его примерно 4,5%, в то время как в окружающем пространстве должно быть около 0,04%. Исследованиями доказано, что даже при достаточном количестве кислорода увеличение доли углекислого газа приводит к появлению головной боли, сонливости, сложности с концентрацией внимания, а при высоком содержании (0,5% и выше) к потере сознания.
В чем измеряется и сколько должно быть
Из-за малых величин концентрацию CO2 обычно выражают в количестве частей на миллион (ppm), что эквивалентно десятитысячным долям процента.
Ниже наименее пугающая картинка из интернета, которая расскажет как повышенная концентрация углекислого газа сказывается на самочувствии. Цифры на шкале — те самые ppm.
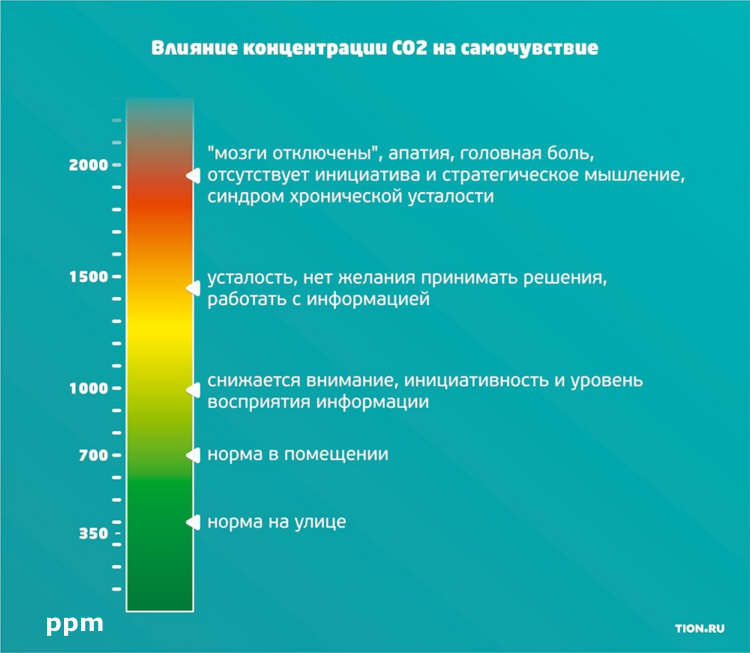
Важный вопрос – сколько может “надышать” человек? В интернете мне удалось найти такую цифру: за один час в закрытом помещении 20 м2 один человек поднимет уровень СО2 на 50 ppm. По моим собственным наблюдениям это вполне похоже не правду.
Ну а теперь к методике и замерам.
Чем измерялось
Все измерения проводились недорогим комнатным прибором HT-501, обзор которого я постил вот тут.

В нем установлен датчик CO2 шведской компании SenseAir. Приборчик может сохранять статистику с заданным интервалом и потом выгружать ее в специальную прогу на ПК. Делая замеры я просто носил прибор в руке или открытой сумке и потом изучал полученные данные.
Сами замеры производились в феврале.
Замеры на улице
В мегаполисе (Москве), если не подходить к дорогам с интенсивным движением, прибор показывает значения в пределах 400-450 ppm. В центре города на тротуарах оживленных улиц показатели могут подняться до 620 ppm.
Замеры в офисе
В нашем просторном опенспейсе с хорошей вентиляцией воздух был примерно как на улице — 450-500 ppm. Но в какой-то из дней вентиляция дала сбой, и типичным значением CO2 стало 950 ppm. Причем к вечеру оно поднималось до 1200 ppm.
Из личных ощущений: как только показатели уходили за 1100 ppm, у окружающих возникало коллективное желание проветрить. После короткого проветривания показатели опускались до 850 ppm.
Замеры в однушке
Если регулярно не проветривать, типичный уровень углекислого газа в квартире 28 м2 и потолками 2,5 м при нахождении в ней двух взрослых колеблется от 800 до 1300 ppm в зависимости от забортной температуры. И чем холоднее на улице, тем лучше начинает работать вентиляция (это в моем доме так, в других может быть по-другому).
Кухня 5,5 м2 с газовой плитой
Кухня — самое интересное место в плане замеров. При закрытой двери одна включенная в полсилы конфорка (на фото ниже) за 15 минут нагоняет более 2300 ppm (вентиляция при этом тянет исправно).

Тот же самый эксперимент, но с открытой дверью и выставленным на зимнее проветривание окном, дает за этот же промежуток времени цифру в 1600 ppm. Ну а если с закрытой дверью и две конфорки — через 15 минут будет 2700 ppm на столе и 3300 ppm на уровне головы в центре помещения.

Комната 15 м2
С закрытой дверью и закрытыми пластиковыми окнами двое взрослых и один ребенок за восемь часов сна поднимают уровень CO2 с 1000 до 2100 ppm. Если оставить окно на зимнее проветривание (щель), то уровень будет стабилизироваться примерно на 1350 ppm. Все то же, но с открытой дверью — 900-1200 ppm.
Почему открытие на зимнее проветривание дает такой заметный эффект? Просто воздух начинает протягиваться из щели окна через комнату и в вентиляцию. Если закрыть щель, комната становится полностью изолированным помещением.
Просто для справки: как себя чувствуешь, когда проснулся, а на датчике 2800 ppm? Духота, жара, тяжелая голова как с похмелья, хочется поскорее выйти на улицу или постоять, подышать у открытого окна.
Замеры в московском метро
Вообще в метро душновато. На станциях и переходах показатели колебались в пределах 750-1250 ppm. Причем день ото дня показатели менялись. В полупустом вагоне “Оки” (все сидячие заняты и немного стоячих) датчик фиксировал примерно 1300 ppm. А в час пик там начинался ад.
Когда люди набивались как селедка в бочку, датчик на уровне пояса стабильно фиксировал 1850 ppm. Поднять его на уровень головы и сделать замеры было уже невозможно. Думаю, он бы зашкаливал, поскольку все вокруг выдыхают именно в верхнее пространство.
Ощущение от нахождения в таких условиях: легкое головокружение, учащенное дыхание и огромное желание выйти и подышать немного. Как люди так катаются каждый день — не представляю.
В подмосковной электричке
В забитом тамбуре гуляют сквозняки, однако уровень CO2 находится примерно на отметке 1400 ppm. В самом вагоне ситуация хуже. При полностью занятых сидячих местах, но в отсутствии стоячих пассажиров, уровень углекислоты составил 2200 ppm.
В автомобиле
В качестве “тестовой площадки” выступал салон старенького Тигуана. В обычных городских поездках с одним водителем в салоне уровень CO2 колебался в пределах 400-600 ppm. В пробках можно было наблюдать примерно 650 ppm. Но самое интересное, разумеется, при включенной рециркуляции воздуха. Ровно за 15 минут CO2 подскакивал с 620 до 1780 единиц! Т.е. рост идет примерно по 80 ppm в минуту и, например, за час он мог бы скакнуть до 4800 единиц. В общем, теперь вы знаете, почему в машине нельзя спать с закрытыми окнами и оставлять в салоне детей или животных. Причем, таких смертельных случаев регистрируется достаточно много. Погуглите…
Выводы: кто виноват и что делать
Эта часть специально для тех, кто начал читать отсюда.
Начнем с общественного транспорта. В нем практически везде душновато, за исключением, пожалуй, маршруток с высокими потолками, где еще можно увидеть приемлемый уровень в 700 ppm.
Очень туго в метро в час пик и ничуть не лучше в электричках. Там зашкаливает даже когда есть сидячие места.
В офисах раз на раз не приходится. И примерно у половины населения опенспейсов возникает желание проветрить, когда уровень начинает превышать 1100 ppm.
В квартире этот уровень воспринимается по-другому, и проветрить хочется когда на датчике более 1300-1400 ppm. И главный совет всем владельцам пластиковых окон — проветривайте почаще, а лучше всегда оставляйте открытой щель зимнего проветривания (это когда ручка повернута градусов на 40 от вертикали).

Это зимой. А летом окна лучше держать открытыми.
Из прочего, самый ад — на кухне с газовыми плитами. Если включена вполсилы пара конфорок и закрыты окна и двери, то через 15 минут на уровне головы будет 3500 ppm. И это при хорошо работающей вентиляции.
Отдельный привет любителям поспать в машине с закрытыми окнами. Очень велик шанс не проснуться. То же можно сказать и про ситуацию, когда вы забыли открыть заслонку забортного воздуха после обгона чадящего грузовика. Показатели в салоне начинают шкалить очень быстро.
Пожалуй, это пока все. Единственное, где я еще хотел бы провести замеры, так это летом в лесу. Надеюсь доживу и проапдейчу данный материал.
P.S. Знаю, что измерители CO2 сейчас есть у многих. Напишите в каментах где и сколько намеряли вы. Но, по возможности, постите не только страшилки.
P.P.S. Тот измеритель CO2, каким пользуюсь я, можно найти на Ali за сумму чуть менее 6 тыс. руб (его обзор тут). Однако за эти же деньги появилась более интересная модель, которая кроме концентрации CO2 может измерять уровень летучей органики (TVOC), концентрацию формальдегида (HCHO) и крупных частиц (PM2.5).
Углекислый газ в атмосфере, его основные источники и поглотители.
Углекислый газ выполняет важную функцию в атмосфере Земли. Он вовлечен в процессы появления и разложения всех живых организмов и образования органических соединений из неорганических.
В биосфере СО2 поддерживает процесс фотосинтеза, который образовывает растительный мир суши и поверхности океана.
Совместно с молекулами воды, метана и озона он формирует «парниковый эффект».

Диоксид углерода — это парниковый газ, который в воздухе воздействует на теплообмен земли и является ключевым элементом в формировании земного климата.
На сегодняшний день прослеживается повышение концентрации двуокиси углерода в атмосфере из-за появления новых искусственных и естественных его источников. Это значит, что климат планеты будет меняться.
Содержание страницы
Источники углекислоты
Большая часть диоксида углерода планеты естественного происхождения. Но также источниками СО2 являются промышленные предприятия и транспорт, которые обеспечивают выброс в атмосферу углекислого газа искусственного происхождения.
Природные источники
При перегнивании деревьев и травы каждый год выделяется 220 миллиардов тонн углекислого газа. Океанами выделяется 330 миллиардов тонн. Пожары, которые образовались в связи с природными факторами приводят к выбросу СО2, равному по количеству антропогенной эмиссии.

Естественными источниками углекислоты являются:
- Дыхание флоры и фауны. Растения и животные поглощают и вырабатывают СО2, так устроено их дыхание.
- Извержение вулканов. Вулканические газы содержат двуокись углерода. В тех регионах, где есть активные вулканы, углекислый газ способен выходить из земных трещин и разломов.
- Разложение органических элементов. Когда органические элементы горят и перегнивают появляется СО2.
Диоксид углерода хранится в углеродных комбинациях: угле, торфе, нефти, известняке. В качестве резервных хранилищ можно назвать океаны, в которых содержатся большие резервы углекислоты и вечную мерзлоту. Однако, вечная мерзлота начинает таять, это можно заметить по уменьшению снежных шапок самых высоких гор мира. При разложении органики наблюдается рост выделения в атмосферу углекислого газа. В результате чего хранилище преобразуется в источник.
Северные районы Аляски, Сибири и Канады — это в основном вечная мерзлота. В ней содержится много органического вещества. Из-за нагрева арктических регионов вечная мерзлота тает и происходит гниение ее содержимого.
Антропогенные источники
Главными искусственными источниками CO2 считаются:

В мире растет количество экологических машин, но их процент по отношению к машинам внутреннего сгорания очень мал. Стоимость электрокаров выше обычных машин, поэтому многие не имеют финансовой возможности приобрести такой вид транспорта.
Интенсивное сокращение лесов для промышленности и сельского хозяйства относится к антропогенным источникам CO2 не в прямом смысле. Деятельность по уменьшению лесных массивов является причиной неучастия диоксида углерода в процессе фотосинтеза. Что приводит к его накоплению в атмосфере.
Поглотители двуокиси углерода
Поглотителями называют любые искусственные или природные системы, которые впитывают из воздуха углекислый газ. Поглотитель — это структура, которая вбирает из воздуха больше CO2 чем выбрасывает в него.
Природные поглотители
Леса способны воздействовать на количество двуокиси углерода в воздухе. Они могут быть и поглотителями, и источниками выбросов параллельно (при вырубке). Когда деревья увеличиваются, а лес растет, то углекислый газ поглощается. Данный процесс считается основой развития биомассы. Выходит, что прогрессирующий лес выступает поглотителем.

Лес северного полушария
При сжигании и уничтожении леса основная доля накопленного углерода опять преобразуется в углекислый газ. В итоге лес снова является источником СО2.
Фитопланктон также является поглотителем углекислого газа на земле. При этом большая часть поглощенного углерода, передаваясь по пищевой цепочке, остается в океане.
Искусственные поглотители
Самыми известными поглотителями СО2 считаются: раствор едкого калия, натронная известь и асбест, едкий натр.
Эти соединения при протекании химических реакций связывают углекислоту, преобразовывая ее в другие соединения. Существуют установки, которые улавливают углекислый газ из выбросов электростанций и преобразуют его в жидкое или твердое состояние с последующим применением в промышленности. Производятся испытания закачки углекислого газа, растворенного в воде, в базальтовые породы под землей. В процессе реакции образуется твердый минерал.

Станция закачки углекислого газа под землю
Взаимодействие с океаном
В океанах углекислота по наличию превышает атмосферное содержание, если пересчитать на углерод, то выйдет примерно 36 триллионов тонн. Растворенный в океане CO2 находится в виде гидрокарбонатов и карбонатов. Эти соединения образуются в процессе химических реакций между подводными скальными породами, водой и двуокисью углерода. Реакции эти обратимы, они вызывают образование известняковых и других карбонатных пород с высвобождением половины гидрокарбонатов в виде диоксида углерода.
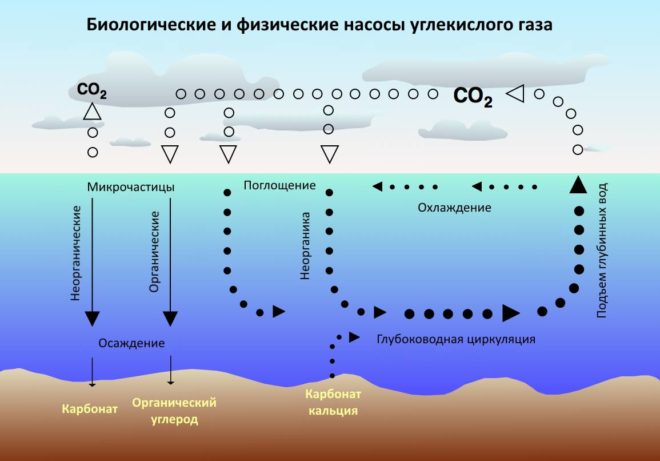
Круговорот углекислого газа в океане
Протекая сотни миллионов лет, этот круговорот реакций привёл к связыванию в карбонатных породах большей части диоксида углерода из атмосферы Земли. По итогу большинство двуокиси углерода, полученной в результате интенсивных выбросов углекислого газа в атмосферу человеком, будет растворено в океанах. Но скорость, с которой будет протекать этот процесс в дальнейшем, остается неизвестной.
Наличие фитопланктона на поверхности океанов помогает поглощать СО2 из воздуха в океан. Некоторое количество углекислого газа фитопланктон поглощает при фотосинтезе, приобретая энергию и источник для развития клеток. Когда он погибает и спускается на дно, углерод остается с ним.
Взаимодействие с землей
Углекислый газ воздуха на генетическом уровне взаимосвязан с землей. Постоянно протекающие почвенные движения увеличивают резервы СО2 в воздухе, где он используется растениями на образование органических элементов. Углекислота выполняет важную функцию в формировании и проветривании почвы. Он принимает участие в разрушении основных минералов, увеличении растворяемости, перемещении карбонатов и фосфатов.
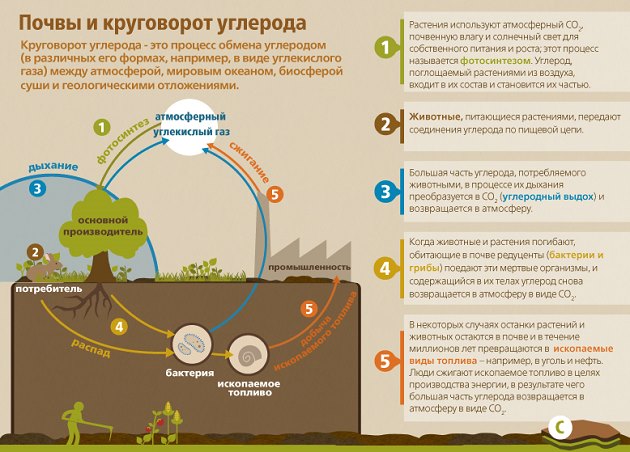
Значительная доля диоксида углерода грунтового воздуха появляется в результате деятельности почвенных организмов, во время распада и окисления органического элемента. До 1/3 части СО2 вырабатывается корнями высоких растений. Также происходит поступление углекислого газа с газами ювенильного и вадозного происхождения из глубочайших шаров земли. В почвах, сформированных на известковых породах, СО2 способен выступать продуктом разрушения углекислого кальция почвенными кислотами.
СО2 грунтового воздуха имеет огромную биологическую значимость. Ее излишек (больше 1%) подавляет проращивание семян и рост корневой системы. Если убрать углекислоту все равно ее кратковременный излишек приведет к медленному росту семян.
В почвах с большим содержанием органического вещества концентрация СО2 летом и весной увеличивается до 3-9 %. Черноземные грунты вырабатывают от 2 до 6 кг углекислого газа на протяжении 24 часов. В почвенном воздухе на глубине 75-150 см в два раза больше содержание СО2 нежели в верхних слоях. В теплые времена содержание СО2 в почвенном воздухе в два раз больше чем в зимний период. Объяснить это можно увеличением активности организмов в грунте.
Необходимо понимать, что многочисленные способы земледелия приводят к повышению концентрации углекислоты в грунте. Среди них можно выделить:
- органические удобрения;
- травосеяние;
- сжатие катками.
Безусловно, не стоит говорить, что плодородность и качество земли зависит исключительно от углекислоты, есть и другие факторы, влияющие на это.
Чтобы регулировать динамику СО2 в почве и увеличивать его содержание до требуемого количества для извлечения хорошего урожая необходимо:
- активировать жизненные процессы в грунте при помощи аэрации;
- осуществлять правильное травосеяние для того чтобы поддерживался и обновлялся резерв органического вещества;
- делать сидерацию и вносить органические удобрения.
Заключение
Несомненно, что без углекислого газа существование на нашей Земле кардинально отличалось бы. Он вовлечен в важнейшие биологические, химические, геологические и климатические процессы. О них важно знать для объяснения многих явлений, происходящих вокруг нас.


 (
(