Нарушение озонового слоя | Экология природных ресурсов
Высоко над Землей, в стратосфере, содержится сравнительно мало известный газ, важный для жизни. Этот газ – озон. Каждая молекула озона состоит из трех атомов кислорода. Озон в стратосфере поглощает больше 99% ультрафиолетового излучения, идущего от Солнца.
Слой озона, или озоновый экран расположен на высоте около 25-45 км. Этот экран предназначен защищать все живое на Земле от жесткого ультрафиолетового излучения. Живые организмы весьма уязвимы для ультрафиолетового излучения, ибо энергии даже одного фотона из этих лучей достаточно, чтобы разрушить химические связи в большинстве органических молекул.
Не случайно поэтому в районах с пониженным содержанием озона многочисленны солнечные ожоги, наблюдается увеличение заболевания людей раком кожи и др. Установлено также, что растения под влиянием сильного ультрафиолетового излучения постепенно теряют свою способность к фотосинтезу, а нарушение жизнедеятельности планктона приводит к разрыву трофических цепей биоты водных экосистем и т.
Истощение озонового слоя
Насыщенность атмосферы озоном постоянно меняется в любой части планеты, достигая максимума весной в приполярной области. Впервые истощение озонового слоя привлекло внимание широкой общественности в 1985 г., когда над Антарктидой было обнаружено пространство с пониженным (до 50%) содержанием озона, по площади соизмеримое с континентальной частью США, получившее название «озоновой дыры».
Позднее блуждающие «озоновые дыры», меньшие по площади и не с таким значительным снижением содержания озона, стали наблюдаться в зимнее время и в Северном полушарии, над Гренландией, северной Канадой и Якутией. Результаты измерений подтверждают повсеместное уменьшение озонового слоя практически на всей планете.
Причины истощения слоя озона
Наука еще до конца не установила, каковы же основные процессы, нарушающие озоновый слой. Ученые выдвинули ряд гипотез как о естественном, так и о техногенном происхождении «озоновых дыр».
Ряд ученых настаивают на естественном происхождении «озоновых дыр». Причины их возникновения одни видят в естественной изменчивости озоносферы, циклической активности Солнца; другие связывают эти процессы с рифтогенезом и дегазацией Земли.
Причины их возникновения одни видят в естественной изменчивости озоносферы, циклической активности Солнца; другие связывают эти процессы с рифтогенезом и дегазацией Земли.
Техногенное происхождение «озоновых дыр» объясняют попаданием в верхние слои атмосферы техногенного хлора, фтора и других атомов и радикалов, способных активно присоединять атомарный кислород, тем самым конкурируя с реакцией:
О + О2= О3.
Так, «озоновые дыры» связывают с тем, что занос активных галогенов в верхние слои атмосферы опосредован летучими хлорфторуглеродами типа фреонов.
Фреоны — фторсодержащие насыщенные углеводороды (главным образом производные метана и этана). Кроме атомов фтора, в молекулах фреонов содержатся обычно атомы хлора, реже — брома. Фреоны широко применяются в промышленном производстве и в быту (хладагенты в холодильниках и кондиционерах, растворители, распылители, аэрозольные упаковки). Фреоны сами по себе не токсичны, инертны, весьма стойки и за счет турбулентных движений с потоком воздуха попадают в стратосферу, где распадаются под действием солнечного УФ с образованием свободного хлора.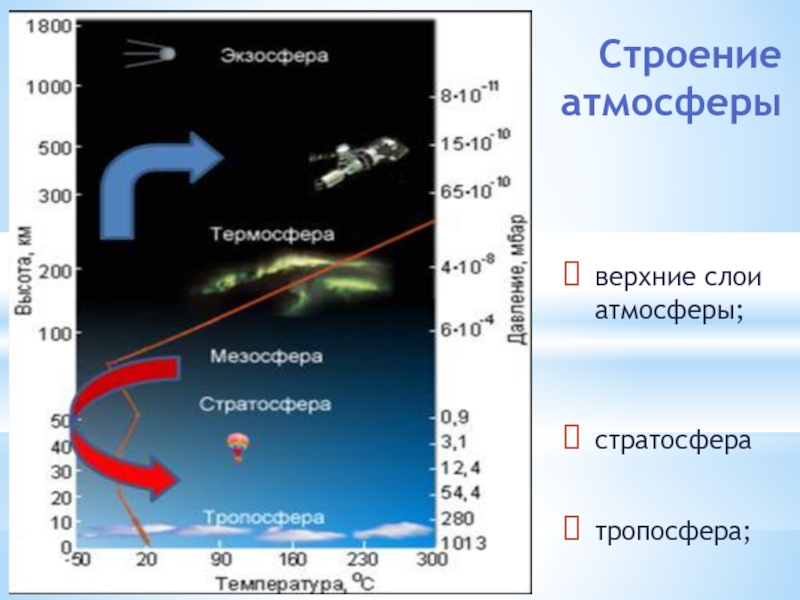 Атомы хлора не сразу вступают в цепную реакцию разрушения озона. Они реагируют с озоном, образуя оксид хлора. Радикалы ClO реагируют друг с другом с образованием относительно стабильного димера ClO — OCl, молекулы которого висят в воздухе, дожидаясь возвращения Солнца.
Атомы хлора не сразу вступают в цепную реакцию разрушения озона. Они реагируют с озоном, образуя оксид хлора. Радикалы ClO реагируют друг с другом с образованием относительно стабильного димера ClO — OCl, молекулы которого висят в воздухе, дожидаясь возвращения Солнца.
Когда наступает антарктическая весна и становится светло, солнечная радиация разрушает димер ClO — OCl, освобождая чрезвычайно реакционноспособный хлор, который начинает взаимодействовать с озоном. Концентрация озона в течение нескольких недель резко падает. По некоторым оценкам, исчезает более 97% озона.
Рефераты
Доклады
Презентации
Вернувшееся солнечное тепло постепенно рассеивает вихрь вокруг полюса, позволяя южному полярному воздуху снова перемешиваться. Обедненный озоном воздух рассеивается по всему земному шару, и уровень озона над Антарктидой становится почти нормальным.
Вследствие длительных запаздываний, необходимых, чтобы молекулы хлорфторуглеродов (ХФУ) достигли стратосферы, дальнейшее истощение озонового слоя неизбежно. Из-за долгого времени жизни в атмосфере молекул ХФУ и атомов хлора оно продлится по меньшей мере 100 лет, даже если производство ХФУ будет повсюду немедленно прекращено.
Из-за долгого времени жизни в атмосфере молекул ХФУ и атомов хлора оно продлится по меньшей мере 100 лет, даже если производство ХФУ будет повсюду немедленно прекращено.
Монреальский протокол
В 1987 г. был принят Монреальский протокол о запрете веществ, разрушающих озоновый слой. В приложении к нему был дан перечень озоноразрушающих веществ (ОРВ), в т.ч. хлорфторуглеродов и бромфторуглеродов.
Монреальский протокол наложил обязательства ограничить потребление, производство, импорт и экспорт ОРВ. В последнее время в США и в ряде западных стран построены заводы по производству новых видов хладореагентов (гидрохлорфторуглеродов) с низким потенциалом разрушения озонового слоя.
К факторам, разрушающим озоновый слой, относят:
- запуски мощных ракет;
- ежедневные полеты реактивных самолетов в высокие слои атмосферы;
- испытания ядерного и термоядерного оружия;
- пожары и вырубка леса — природного озонатора.
Основные мероприятия по охране атмосферного воздуха >
Разрушение озонового слоя: причины и последствия: Статьи экологии ➕1, 07.
 06.2022
06.2022Озоновый слой — это часть стратосферы Земли, поглощающая избыток ультрафиолетового излучения. Но эта защита не безупречна. Plus-one.ru — о том, из-за чего разрушается озоновый слой и к каким последствиям это может привести.
Фото: iStock
Озоновую дыру впервые обнаружили в 1985 году над Антарктидой. Она появлялась весной, а когда ветры начинали дуть в другом направлении, заполнялась молекулами O3 из соседних участков атмосферы. Но даже в этот период проблема не исчезала, так как края дыры постепенно истончались и теряли способность эффективно сдерживать ультрафиолетовое излучение.
Научные исследования подтвердили, что озоновый слой повреждается из-за использования химикатов, содержащих хлор и бром. Их также называют озоноразрушающими веществами (ОРВ). Широкое использование ОРВ объяснялось их нетоксичностью и стабильностью. Но именно стабильность этих веществ оказалась губительной для экологии.
ОРВ поднимаются до уровня стратосферы и задерживаются там, распадаясь под воздействием УФ-лучей. Этот процесс сопровождается выделением хлора и брома, расщепляющих молекулы O3 на атомы. ОРВ способны накапливаться в атмосфере. Значительная часть веществ, использовавшихся человеком в течение последних нескольких десятков лет, все еще оказывает разрушающее воздействие на озоновый слой. Так, доказано, что молекула хлора покидает атмосферу нашей планеты лишь спустя 75-111 лет.
Истончение озонового слоя, в борьбе с которым с 1980-х годов были достигнуты значительные успехи, усиливается из-за глобального потепления. В 2019 году в районе Арктики образовалась озоновая дыра, площадь которой втрое больше территории Гренландии. Ее появление связано не только с выбросами химикатов, но и с изменением климата. Из-за ослабления действия полярных вихрей в районе Северного полюса скопились массы охлажденного воздуха. Их объем был больше, чем в 1937 году, когда зима была рекордно холодной. Это привело к образованию стратосферных облаков, удерживающих вредные вещества вблизи озоносферы.
Это привело к образованию стратосферных облаков, удерживающих вредные вещества вблизи озоносферы.
Как украинский кризис повлиял на борьбу с глобальным потеплением
Насколько опасно промедление, вызванное санкциями против России и энергетическим коллапсом
80% повреждений озоносферы связано с использованием ОРВ. К ним относятся:
Хлорфторуглероды (ХФУ). Используются при производстве аэрозолей, пен, растворителей, хладагентов для кондиционеров, холодильного оборудования, веществ для стерилизации хирургических инструментов.
Тетрахлорметан. Это сырье для медикаментов и сельскохозяйственных химикатов, растворитель смол, жиров, каучука и других веществ. Также тетрахлорметан необходим для получения фреонов.
Бромистый метил. Применяется в пищевой и сельскохозяйственной промышленности. Позволяет бороться с бактериями, грибками, насекомыми, грызунами и поражающими растения вирусами.
Для сохранения озонового слоя эти вещества заменяют аналогами, не оказывающими разрушительного воздействия на молекулы O3. Например, альтернативой галонам служат инертные газы, галоидоуглеводороды, потоковые агенты, водяной туман, тонкодисперсные частицы аэрозолей.
Озон — это одна из самых важных составляющих земной атмосферы. Он поглощает ультрафиолетовое излучение солнца, высокие дозы которого губительны для всего живого. Под воздействием УФ-лучей нарушается зрение, снижается способность организма сопротивляться инфекциям. Люди чаще страдают от аллергических реакций, онкологии, преждевременного старения, кожных заболеваний, неврозов. Так, среднегодовой прирост заболеваемости меланомой — наиболее опасной формой рака кожи — в России составляет 3,9%, в США — 6%. При этом 86% случаев этой патологии связано с воздействием УФ-лучей.
Фото: iStock
Кроме того, ультрафиолетовые лучи подавляют процесс фотосинтеза растений. А токсичные сине-зеленые водоросли, наоборот, под их воздействием начинают активно развиваться, ухудшая условия жизни обитателей водоемов. Излучение способно поражать икру и мальков рыб, а также устриц, крабов и других мелких животных. Рыболовство поставляет около 20% белка, потребляемого в мире, поэтому обеспечение человечества продовольствием находится под угрозой.
А токсичные сине-зеленые водоросли, наоборот, под их воздействием начинают активно развиваться, ухудшая условия жизни обитателей водоемов. Излучение способно поражать икру и мальков рыб, а также устриц, крабов и других мелких животных. Рыболовство поставляет около 20% белка, потребляемого в мире, поэтому обеспечение человечества продовольствием находится под угрозой.
Проблема озонового слоя отражается и на плодородии почв. В верхнем слое грунта обитают цианобактерии. Они синтезируют органические вещества, необходимые для роста растений, и участвуют в процессе самоочищения почвы от загрязнений. Ультрафиолетовое излучение нарушает эти процессы, блокируя действие фермента нитрогеназы, необходимого бактериям для преобразования атмосферного азота в удобрение.
Еще одна важная роль озона для биосферы — поддержание нужной концентрации кислорода в воздухе. Молекулы O3 динамичны и могут перемещаться в разных направлениях. Когда озон выходит за пределы защитного экрана, его замещает кислород.
В 1977 году в Вашингтоне представители 32 государств разработали первый план действий по защите озоносферы. В итоге в США, Норвегии, Швеции и Канаде запретили использование аэрозолей с хлорфторуглеродами. Но решение проблемы озонового слоя требовало более глобальных действий.
22 мая 1985 года члены ООН сделали следующий шаг на пути к защите земной атмосферы, приняв Венскую конвенцию об охране озонового слоя. Это экологическое соглашение вступило в силу в 1988 году. Оно послужило стимулом для международных усилий по снижению концентрации ОРВ, но не поставило перед участниками конкретные цели. Конвенцию ратифицировали 120 стран и ЕЭС — Европейское экономическое сообщество, состоявшее из 12 государств и существовавшее с 1957-го по 1993 год. Советский Союз присоединился к конвенции в 1986-м.
16 сентября 1987 года был принят Монреальский протокол по озоноразрушающим веществам. Документ подписали представители 46 стран, в том числе Советского Союза. В 1994 году ООН провозгласила дату заключения этого договора Международным днем охраны озонового слоя.
В 1994 году ООН провозгласила дату заключения этого договора Международным днем охраны озонового слоя.
К 2011 году государства-участники Монреальского протокола сократили объем использования веществ из утвержденного перечня на 98%. По данным NASA, озоновая дыра над Антарктидой с 1980-х годов постепенно затягивается. Правда, при низких температурах ее границы временно расширяются, так как часть вредных веществ еще не покинула атмосферу. Прогнозируется, что к 2040 году концентрация ОРВ в воздухе снизится настолько, что погодные условия больше не будут влиять на разрушение O3.
Состояние озоновой дыры над Антарктидой с 1 июля по 31 декабря в период с 1979-го по 2018 год, видео NASA
В октябре 2016 года сторонами Монреальского протокола была принята Кигалийская поправка. Она призывает страны поэтапно отказаться от использования гидрофторуглеродов, также называемых сверхпарниковыми газами. Эта мера направлена как на защиту озонового слоя, так и на снижение темпов глобального потепления. В России эта поправка начала действовать с 1 января 2021 года. К 2036 году запланировано сократить использование ГФУ на 85%. Вице-премьер правительства РФ Виктория Абрамченко отметила, что такой плавный переход позволит производствам адаптироваться к использованию альтернативных хладагентов, в том числе природного происхождения.
В России эта поправка начала действовать с 1 января 2021 года. К 2036 году запланировано сократить использование ГФУ на 85%. Вице-премьер правительства РФ Виктория Абрамченко отметила, что такой плавный переход позволит производствам адаптироваться к использованию альтернативных хладагентов, в том числе природного происхождения.
Помимо этого, в 2022 году в нашей стране планируется на 20% снизить объем ОРВ по сравнению с 2021 годом. Список разрешенных веществ из этой группы ограничили двумя наименованиями. Допустимый уровень потребления дифторхлорметана — 218,6 тонны, фтордихлорэтана — 72,3 тонны.
Подписывайтесь на наш канал в Яндекс.Дзен.
Автор
Вера Жихарева
Основы изучения озонового слоя | US EPA
Озоновый слой Земли Область стратосферы, содержащая основную часть атмосферного озона. Озоновый слой находится примерно на высоте 15-40 километров (10-25 миль) над поверхностью Земли, в стратосфере. Истощение этого слоя озоноразрушающими веществами (ОРВ) приведет к повышению уровня УФ-В, что, в свою очередь, приведет к увеличению числа случаев рака кожи и катаракты, а также к потенциальному повреждению некоторых морских организмов, растений и пластмасс. Научная страница (http://www.epa.gov/ozone/science/index.html) предлагает более подробную информацию о науке об истощении озонового слоя. защищает все живое от вредного солнечного излучения, но деятельность человека повредила этот щит. Меньшая защита озонового слоя от ультрафиолетовый (УФ) свет Ультрафиолетовое излучение представляет собой часть электромагнитного спектра с длинами волн короче видимого света. Солнце излучает ультрафиолет, который обычно делится на три диапазона: UVA, UVB и UVC. UVA не поглощается озоном. UVB в основном поглощается озоном, хотя некоторые из них достигают Земли. UVC полностью поглощается озоном и нормальным кислородом. НАСА предоставляет дополнительную информацию на своем веб-сайте (http://www.
Истощение этого слоя озоноразрушающими веществами (ОРВ) приведет к повышению уровня УФ-В, что, в свою очередь, приведет к увеличению числа случаев рака кожи и катаракты, а также к потенциальному повреждению некоторых морских организмов, растений и пластмасс. Научная страница (http://www.epa.gov/ozone/science/index.html) предлагает более подробную информацию о науке об истощении озонового слоя. защищает все живое от вредного солнечного излучения, но деятельность человека повредила этот щит. Меньшая защита озонового слоя от ультрафиолетовый (УФ) свет Ультрафиолетовое излучение представляет собой часть электромагнитного спектра с длинами волн короче видимого света. Солнце излучает ультрафиолет, который обычно делится на три диапазона: UVA, UVB и UVC. UVA не поглощается озоном. UVB в основном поглощается озоном, хотя некоторые из них достигают Земли. UVC полностью поглощается озоном и нормальным кислородом. НАСА предоставляет дополнительную информацию на своем веб-сайте (http://www. nas.nasa.gov/About/Education/Ozone/radiation.html). со временем нанесет ущерб посевам и приведет к более высокому уровню рака кожи и катаракты.
nas.nasa.gov/About/Education/Ozone/radiation.html). со временем нанесет ущерб посевам и приведет к более высокому уровню рака кожи и катаракты.
Ключевые ресурсы
Научная оценка истощения озонового слоя: 2018
I. Озоновый слой
Атмосфера Земли состоит из нескольких слоев. Самый нижний слой, тропосфера Ближайшая к Земле область атмосферы. Тропосфера простирается от поверхности примерно до 10 км в высоту, хотя эта высота меняется в зависимости от широты. Почти вся погода происходит в тропосфере. Гора Эверест, самая высокая гора на Земле, имеет высоту всего 8,8 км. Температура в тропосфере снижается с высотой. По мере того, как теплый воздух поднимается вверх, он охлаждается, опускаясь обратно на Землю. Этот процесс, известный как конвекция, означает, что существуют огромные движения воздуха, которые очень эффективно перемешивают тропосферу. Он простирается от поверхности Земли на высоту примерно до 6 миль или 10 километров (км). Практически вся деятельность человека происходит в тропосфере. Гора Эверест, самая высокая гора на планете, составляет всего около 5,6 миль (9км) высокая. Следующий слой, стратосфера Область атмосферы выше тропосферы. Стратосфера простирается на высоте от 10 до 50 км. Коммерческие авиалинии летают в нижней стратосфере. Стратосфера становится теплее на больших высотах. На самом деле это потепление вызвано тем, что озон поглощает ультрафиолетовое излучение. Теплый воздух остается в верхней стратосфере, а холодный воздух остается ниже, поэтому вертикальное перемешивание в этом регионе гораздо меньше, чем в тропосфере, продолжается от 6 миль (10 км) до примерно 31 мили (50 км). Большинство коммерческих самолетов летают в нижней части стратосферы.
Гора Эверест, самая высокая гора на планете, составляет всего около 5,6 миль (9км) высокая. Следующий слой, стратосфера Область атмосферы выше тропосферы. Стратосфера простирается на высоте от 10 до 50 км. Коммерческие авиалинии летают в нижней стратосфере. Стратосфера становится теплее на больших высотах. На самом деле это потепление вызвано тем, что озон поглощает ультрафиолетовое излучение. Теплый воздух остается в верхней стратосфере, а холодный воздух остается ниже, поэтому вертикальное перемешивание в этом регионе гораздо меньше, чем в тропосфере, продолжается от 6 миль (10 км) до примерно 31 мили (50 км). Большинство коммерческих самолетов летают в нижней части стратосферы.
Большая часть атмосферного озона сосредоточена в слое стратосферы на высоте от 9 до 18 миль (от 15 до 30 км) над поверхностью Земли (см. рисунок ниже). Озон — это молекула, содержащая три атома кислорода. В любой момент времени в стратосфере постоянно образуются и разрушаются молекулы озона.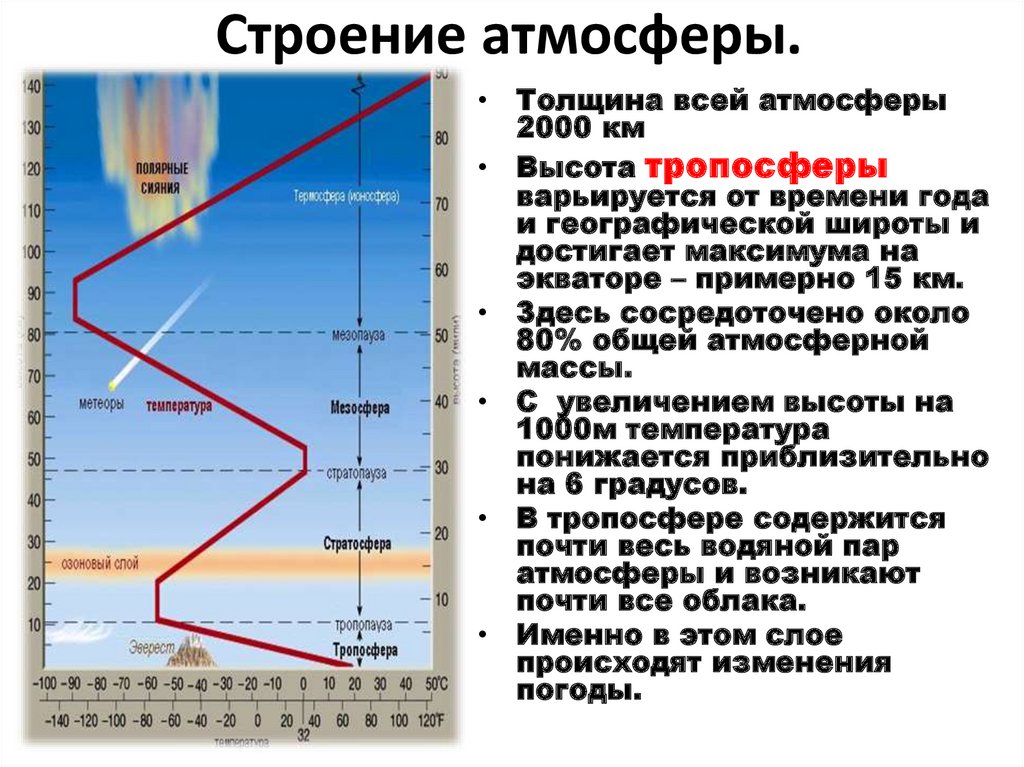
Озоновый слой в стратосфере поглощает часть солнечной радиации, не давая ей достичь поверхности планеты. Что наиболее важно, он поглощает часть УФ-излучения, называемую UVB Полоса ультрафиолетового излучения с длиной волны от 280 до 320 нанометров, создаваемая Солнцем. UVB — это разновидность ультрафиолетового излучения солнца (и солнечных ламп), которое имеет несколько вредных эффектов. UVB особенно эффективно повреждает ДНК. Это причина меланомы и других видов рака кожи. Он также был связан с повреждением некоторых материалов, сельскохозяйственных культур и морских организмов.
Ученые установили записи за несколько десятилетий, в которых подробно описаны нормальные уровни озона во время естественных циклов. Концентрации озона в атмосфере естественным образом меняются в зависимости от солнечных пятен, времен года и широты. Эти процессы хорошо изучены и предсказуемы. Каждое естественное снижение уровня озона сопровождалось восстановлением.
II. Истощение озонового слоя
Когда атомы хлора и брома вступают в контакт с озоном в стратосфере, они разрушают молекулы озона. Один атом хлора может разрушить более 100 000 молекул озона, прежде чем он будет удален из стратосферы. Озон может быть уничтожен быстрее, чем он образуется естественным путем.
Некоторые соединения выделяют хлор или бром при воздействии интенсивного ультрафиолетового излучения в стратосфере. Эти соединения способствуют разрушению озонового слоя и называются озоноразрушающими веществами (9).0003 ODS Соединение, способствующее разрушению стратосферного озона. ОРВ включают хлорфторуглероды (ХФУ), гидрохлорфторуглероды (ГХФУ), галоны, бромистый метил, четыреххлористый углерод, гидробромфторуглероды, хлорбромметан и метилхлороформ. ОРВ, как правило, очень стабильны в тропосфере и разлагаются только под воздействием интенсивного ультрафиолетового света в стратосфере.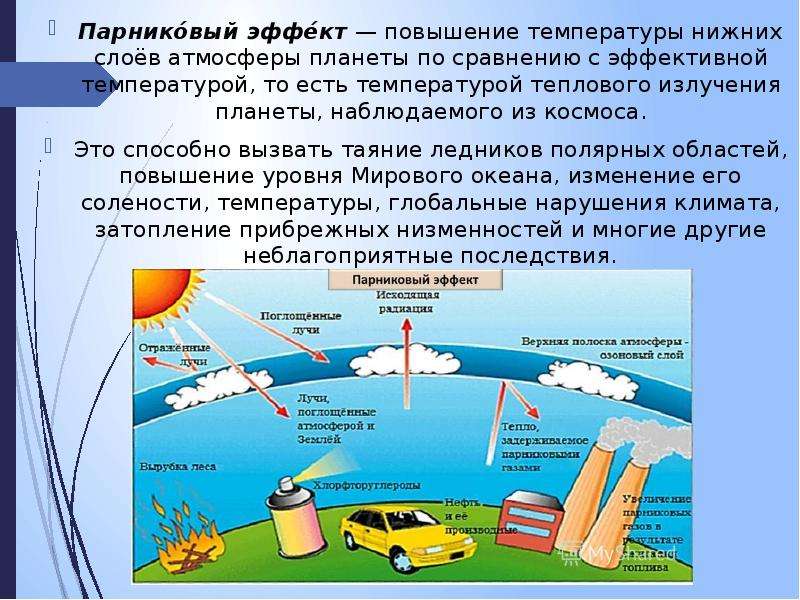 Когда они распадаются, они выделяют атомы хлора или брома, которые затем разрушают озон. Доступен подробный список (http://www.epa.gov/ozone/science/ods/index.html) веществ класса I и класса II с их ODP, GWP и номерами CAS). ОРВ, выделяющие хлор, включают хлорфторуглероды Газы, подпадающие под действие Монреальского протокола 1987 года и используемые для охлаждения, кондиционирования воздуха, упаковки, изоляции, растворителей или аэрозольных пропеллентов. Поскольку они не разрушаются в нижних слоях атмосферы, ХФУ дрейфуют в верхние слои атмосферы, где при подходящих условиях разрушают озон. Эти газы заменяются другими соединениями: гидрохлорфторуглеродами, временной заменой ХФУ, которые также подпадают под действие Монреальского протокола, и гидрофторуглеродами, подпадающими под действие Киотского протокола. Все эти вещества также являются парниковыми газами. См. гидрохлорфторуглероды, гидрофторуглероды, перфторуглероды, вещества, разрушающие озоновый слой. (ХФУ), Гидрохлорфторуглероды Соединения, содержащие атомы водорода, фтора, хлора и углерода.
Когда они распадаются, они выделяют атомы хлора или брома, которые затем разрушают озон. Доступен подробный список (http://www.epa.gov/ozone/science/ods/index.html) веществ класса I и класса II с их ODP, GWP и номерами CAS). ОРВ, выделяющие хлор, включают хлорфторуглероды Газы, подпадающие под действие Монреальского протокола 1987 года и используемые для охлаждения, кондиционирования воздуха, упаковки, изоляции, растворителей или аэрозольных пропеллентов. Поскольку они не разрушаются в нижних слоях атмосферы, ХФУ дрейфуют в верхние слои атмосферы, где при подходящих условиях разрушают озон. Эти газы заменяются другими соединениями: гидрохлорфторуглеродами, временной заменой ХФУ, которые также подпадают под действие Монреальского протокола, и гидрофторуглеродами, подпадающими под действие Киотского протокола. Все эти вещества также являются парниковыми газами. См. гидрохлорфторуглероды, гидрофторуглероды, перфторуглероды, вещества, разрушающие озоновый слой. (ХФУ), Гидрохлорфторуглероды Соединения, содержащие атомы водорода, фтора, хлора и углерода. Хотя вещества разрушают озоновый слой, они менее эффективны в разрушении стратосферного озона, чем хлорфторуглероды (ХФУ). Они были введены в качестве временной замены ХФУ и также являются парниковыми газами. См. вещество, разрушающее озоновый слой. (ГХФУ), четыреххлористый углерод Соединение, состоящее из одного атома углерода и четырех атомов хлора. Четыреххлористый углерод широко использовался в качестве сырья во многих отраслях промышленности, включая производство хлорфторуглеродов (ХФУ), а также в качестве растворителя. Использование растворителей прекратилось, когда было обнаружено, что они канцерогенны. Он также используется в качестве катализатора для доставки ионов хлора в определенные процессы. Его озоноразрушающий потенциал составляет 1,2, а метилхлороформ Соединение, состоящее из углерода, водорода и хлора. Метилхлороформ используется в качестве промышленного растворителя. Его озоноразрушающий потенциал составляет 0,11. ОРВ, выделяющие бром, включают галона соединений, также известных как бромфторуглероды, которые содержат бром, фтор и углерод.
Хотя вещества разрушают озоновый слой, они менее эффективны в разрушении стратосферного озона, чем хлорфторуглероды (ХФУ). Они были введены в качестве временной замены ХФУ и также являются парниковыми газами. См. вещество, разрушающее озоновый слой. (ГХФУ), четыреххлористый углерод Соединение, состоящее из одного атома углерода и четырех атомов хлора. Четыреххлористый углерод широко использовался в качестве сырья во многих отраслях промышленности, включая производство хлорфторуглеродов (ХФУ), а также в качестве растворителя. Использование растворителей прекратилось, когда было обнаружено, что они канцерогенны. Он также используется в качестве катализатора для доставки ионов хлора в определенные процессы. Его озоноразрушающий потенциал составляет 1,2, а метилхлороформ Соединение, состоящее из углерода, водорода и хлора. Метилхлороформ используется в качестве промышленного растворителя. Его озоноразрушающий потенциал составляет 0,11. ОРВ, выделяющие бром, включают галона соединений, также известных как бромфторуглероды, которые содержат бром, фтор и углерод. Они обычно используются в качестве средств пожаротушения и вызывают разрушение озонового слоя. Бром во много раз эффективнее разрушает стратосферный озон, чем хлор. См. вещество, разрушающее озоновый слой. и бромистый метил Соединение, состоящее из углерода, водорода и брома. Метилбромид — эффективный пестицид, используемый для фумигации почвы и многих сельскохозяйственных продуктов. Поскольку он содержит бром, он разрушает стратосферный озон и имеет озоноразрушающий потенциал 0,6. Производство бромистого метила было прекращено 31 декабря 2004 г., за исключением допустимых исключений. Доступно гораздо больше информации (http://www.epa.gov/ozone/mbr/index.html). Хотя ОРВ выбрасываются на поверхность Земли, в конечном итоге они попадают в стратосферу в процессе, который может занять от двух до пяти лет.
Они обычно используются в качестве средств пожаротушения и вызывают разрушение озонового слоя. Бром во много раз эффективнее разрушает стратосферный озон, чем хлор. См. вещество, разрушающее озоновый слой. и бромистый метил Соединение, состоящее из углерода, водорода и брома. Метилбромид — эффективный пестицид, используемый для фумигации почвы и многих сельскохозяйственных продуктов. Поскольку он содержит бром, он разрушает стратосферный озон и имеет озоноразрушающий потенциал 0,6. Производство бромистого метила было прекращено 31 декабря 2004 г., за исключением допустимых исключений. Доступно гораздо больше информации (http://www.epa.gov/ozone/mbr/index.html). Хотя ОРВ выбрасываются на поверхность Земли, в конечном итоге они попадают в стратосферу в процессе, который может занять от двух до пяти лет.
В 1970-х годах опасения по поводу воздействия озоноразрушающих веществ ( ОРВ Соединение, которое способствует разрушению стратосферного озона. ОРВ включают хлорфторуглероды (ХФУ), гидрохлорфторуглероды (ГХФУ), галоны, бромистый метил, четыреххлористый углерод, гидробромфторуглероды, хлорбромметан и метил хлороформ. ОРВ, как правило, очень стабильны в тропосфере и разлагаются только под интенсивным ультрафиолетовым излучением в стратосфере. При распаде они выделяют атомы хлора или брома, которые затем разрушают озон. Доступен подробный список (http://www.epa.gov/ozone/science/ods/index.html) веществ класса I и класса II с указанием их ОРП, ПГП и номеров CAS.) в стратосфере озоновый слой Область стратосферы, содержащая основную часть атмосферного озона. Озоновый слой находится примерно на высоте 15-40 километров (10-25 миль) над поверхностью Земли, в стратосфере. Истощение этого слоя озоноразрушающими веществами (ОРВ) приведет к повышению уровня УФ-В, что, в свою очередь, приведет к увеличению числа случаев рака кожи и катаракты, а также к потенциальному повреждению некоторых морских организмов, растений и пластмасс. Научная страница (http://www.epa.gov/ozone/science/index.html) предлагает более подробную информацию о науке об истощении озонового слоя. побудил несколько стран, в том числе США, запретить использование хлорфторуглеродов ( ХФУ Органические соединения, состоящие из атомов углерода, хлора и фтора.
ОРВ, как правило, очень стабильны в тропосфере и разлагаются только под интенсивным ультрафиолетовым излучением в стратосфере. При распаде они выделяют атомы хлора или брома, которые затем разрушают озон. Доступен подробный список (http://www.epa.gov/ozone/science/ods/index.html) веществ класса I и класса II с указанием их ОРП, ПГП и номеров CAS.) в стратосфере озоновый слой Область стратосферы, содержащая основную часть атмосферного озона. Озоновый слой находится примерно на высоте 15-40 километров (10-25 миль) над поверхностью Земли, в стратосфере. Истощение этого слоя озоноразрушающими веществами (ОРВ) приведет к повышению уровня УФ-В, что, в свою очередь, приведет к увеличению числа случаев рака кожи и катаракты, а также к потенциальному повреждению некоторых морских организмов, растений и пластмасс. Научная страница (http://www.epa.gov/ozone/science/index.html) предлагает более подробную информацию о науке об истощении озонового слоя. побудил несколько стран, в том числе США, запретить использование хлорфторуглеродов ( ХФУ Органические соединения, состоящие из атомов углерода, хлора и фтора. Примером является CFC-12 (CCI2F2), используемый в качестве хладагента в холодильниках и кондиционерах, а также в качестве пенообразователя. Газообразные фреоны могут разрушать озоновый слой, когда они медленно поднимаются в стратосферу, разрушаются сильным ультрафиолетовым излучением, высвобождают атомы хлора, а затем реагируют с молекулами озона. См. Вещество, разрушающее озоновый слой.) как аэрозоль Небольшая капля или частица, взвешенная в атмосфере, обычно содержащая серу. Аэрозоли выбрасываются естественным образом (например, при извержении вулканов) и в результате деятельности человека (например, при сжигании ископаемого топлива). Нет никакой связи между аэрозолями в виде твердых частиц и продуктами под давлением, также называемыми аэрозолями. (См. ниже) пропелленты. Тем не менее, мировое производство ХФУ и других ОРВ продолжало быстро расти по мере того, как эти химические вещества находили новые применения в холодильной технике, пожаротушении, пеноизоляции и других областях применения.
Примером является CFC-12 (CCI2F2), используемый в качестве хладагента в холодильниках и кондиционерах, а также в качестве пенообразователя. Газообразные фреоны могут разрушать озоновый слой, когда они медленно поднимаются в стратосферу, разрушаются сильным ультрафиолетовым излучением, высвобождают атомы хлора, а затем реагируют с молекулами озона. См. Вещество, разрушающее озоновый слой.) как аэрозоль Небольшая капля или частица, взвешенная в атмосфере, обычно содержащая серу. Аэрозоли выбрасываются естественным образом (например, при извержении вулканов) и в результате деятельности человека (например, при сжигании ископаемого топлива). Нет никакой связи между аэрозолями в виде твердых частиц и продуктами под давлением, также называемыми аэрозолями. (См. ниже) пропелленты. Тем не менее, мировое производство ХФУ и других ОРВ продолжало быстро расти по мере того, как эти химические вещества находили новые применения в холодильной технике, пожаротушении, пеноизоляции и других областях применения.
Некоторые естественные процессы, такие как крупные извержения вулканов, могут косвенно влиять на уровень озона. Например, извержение горы Пинатубо в 1991 году не привело к увеличению концентрации хлора в стратосфере, но оно произвело большое количество крошечных частиц, называемых аэрозолями Мелкие частицы или жидкие капли в атмосфере, которые могут поглощать или отражать солнечный свет в зависимости от их состава. (в отличие от потребительских товаров, также известных как аэрозоли). Эти аэрозоли повышают эффективность хлора при разрушении озона. Аэрозоли в стратосфере создают поверхность, на которой хлор на основе ХФУ может разрушать озон. Однако эффект от вулканов недолговечен.
Не все источники хлора и брома способствуют разрушению озонового слоя. Например, исследователи обнаружили, что хлор из бассейнов, промышленных предприятий, морской соли и вулканов не достигает стратосферы. Напротив, ОРВ очень стабильны и не растворяются в дожде. Таким образом, отсутствуют естественные процессы, удаляющие ОРВ из нижних слоев атмосферы.
Одним из примеров истощения озонового слоя является ежегодная озоновая «дыра» над Антарктидой, которая образуется во время антарктической весны с начала 19 века.80-е годы. На самом деле это не дыра в озоновом слое, а большая область стратосферы с крайне низким содержанием озона.
Истощение озонового слоя не ограничивается районом над Южным полюсом. Исследования показали, что истощение озонового слоя происходит на широтах, включающих Северную Америку, Европу, Азию и большую часть Африки, Австралии и Южной Америки. Дополнительную информацию о глобальных масштабах разрушения озонового слоя можно найти в документе «Научная оценка разрушения озонового слоя: 2018 г.» разработан Программой ООН по окружающей среде.
Хлорфторуглероды и разрушение озонового слоя — Американское химическое общество
- Вы здесь:
- СКУД
- Студенты и преподаватели
- Исследуйте химию
- Химические достопримечательности
- Хлорфторуглероды и разрушение озонового слоя
Национальная историческая химическая достопримечательность
En español: Los cloroluminocarbonos y el agujero de ozono
Выделен Калифорнийскому университету в Ирвине 18 апреля 2017 г.
язык сух и академичен, как и подобает реферату научной статьи в престижном журнале Nature . Однако исследование, описанное в короткой статье, произвело эффект разорвавшейся бомбы, последствия которой будут ощущаться во всем мире. Это вызвало ожесточенные дебаты, привело к глобальному экологическому соглашению, ограничивающему использование широкого класса химических веществ, и изменило отношение людей к их влиянию на окружающую среду Земли. Это также привело к Ф. Шервуду Роуленду (1927-2012) и Марио Дж. Молина (*1943), получивший Нобелевскую премию по химии 1995 года вместе с Полом Дж. Круценом из Института химии им. Макса Планка в Майнце, еще одним пионером в исследованиях стратосферного озона.
Роуленд, профессор химии Калифорнийского университета в Ирвине, и Молина, научный сотрудник лаборатории Роуленда, показали, что хлорфторуглероды — ХФУ — могут разрушать озон, молекулу, состоящую из трех атомов кислорода, O 3 , в стратосфере Земли. Этот стратосферный озон поглощает ультрафиолетовое излучение, которое в противном случае достигло бы поверхности Земли. В то время ХФУ широко использовались в холодильной технике, кондиционерах и аэрозольных баллончиках. Соединения инертны и практически нетоксичны, что делает их хорошо подходящими для этих применений. Однако эти же характеристики также делали их опасными для жизни на Земле.
В то время ХФУ широко использовались в холодильной технике, кондиционерах и аэрозольных баллончиках. Соединения инертны и практически нетоксичны, что делает их хорошо подходящими для этих применений. Однако эти же характеристики также делали их опасными для жизни на Земле.
Памятный буклет (PDF)
Ориентировочный план урока: Хлорфторуглероды и разрушение озонового слоя
Содержание
- Широкое использование ХФУ
- Значение озона
- От исследований к сопротивлению
- Антарктическая озоновая дыра
- Знаковое посвящение и благодарность
- Дополнительные ресурсы
Широкое использование ХФУ
В 1920-х годах в системах охлаждения и кондиционирования воздуха в качестве хладагентов использовались такие соединения, как аммиак, хлорметан, пропан и диоксид серы. Несмотря на эффективность, соединения были токсичными и легковоспламеняющимися, и их воздействие могло привести к серьезным травмам или смерти. Группа химиков Frigidaire под руководством Томаса Миджли-младшего (1889–1944) работала над созданием нетоксичных и негорючих альтернатив хладагентам.
Группа химиков Frigidaire под руководством Томаса Миджли-младшего (1889–1944) работала над созданием нетоксичных и негорючих альтернатив хладагентам.
Группа сосредоточила свои усилия на соединениях, содержащих углерод и галогены, такие как фтор и хлор. Известно, что такие соединения летучи и химически инертны, что является важным свойством для группы, изучающей их использование в холодильной технике. Первым соединением, которое они разработали, был дихлордифторметан, CCl 9.0101 2 F 2 , который они назвали «Фреоном». Миджли получит медаль Перкина Общества химической промышленности за это исследование в 1937 году; в 1941 году он был награжден медалью Пристли, высшей наградой Американского химического общества, за вклад в химию.
К началу 1970-х годов ХФУ получили широкое распространение, и мировое производство соединений достигло почти одного миллиона тонн в год, что составляет примерно 500 миллионов долларов в химической промышленности.
К началу страницы
Хлорфторметаны попадают в окружающую среду в неуклонно возрастающих количествах. Эти соединения химически инертны и могут оставаться в атмосфере в течение 40–150 лет, а их концентрации, как ожидается, превысят нынешние уровни в 10–30 раз. Фотодиссоциация хлорфторметанов в стратосфере производит значительное количество атомов хлора и приводит к разрушению атмосферного озона».
Эти соединения химически инертны и могут оставаться в атмосфере в течение 40–150 лет, а их концентрации, как ожидается, превысят нынешние уровни в 10–30 раз. Фотодиссоциация хлорфторметанов в стратосфере производит значительное количество атомов хлора и приводит к разрушению атмосферного озона».
—Ф. Шервуд Роуленд и Марио Дж. Молина, 9 лет0097 Nature , 1974
Важность озона
С экологической точки зрения озон представляет собой загадочную молекулу. В тропосфере, области атмосферы от поверхности Земли до примерно 6 миль, озон является загрязнителем, который является компонентом фотохимического смога. Но в стратосфере, области атмосферы от 6 до 31 мили, озон поглощает потенциально вредное ультрафиолетовое (УФ) излучение.
Как заявила Шведская королевская академия наук в своем объявлении о 1995 Нобелевская премия по химии: «Хотя озон встречается в таких малых количествах, он играет исключительно важную роль в жизни на Земле. Это связано с тем, что озон вместе с обычным молекулярным кислородом (O 2 ) способен поглощать большую часть солнечного ультрафиолетового излучения и тем самым предотвращать попадание этого опасного излучения на поверхность. Без защитного озонового слоя в атмосфере животные и растения не могли бы существовать, по крайней мере, на суше».
Без защитного озонового слоя в атмосфере животные и растения не могли бы существовать, по крайней мере, на суше».
Интерес Роуленда к судьбе ХФУ в атмосфере был вызван докладом, который он услышал на конференции в 1972. Докладчик обсудил результаты, полученные Джеймсом Лавлоком (*1919 г.), британским ученым, который изобрел высокочувствительный способ измерения следовых газов. Лавлок измерил количество трихлорфторметана (ХФУ-11) в атмосфере, которое предполагало, что практически весь когда-либо произведенный ХФУ-11 все еще присутствует в атмосфере.
Роуленд решил посвятить часть своих исследований изучению судьбы фреонов в атмосфере. Хотя ХФУ инертны в нижних слоях тропосферы, Роуленд понял, что они могут быть разрушены УФ-излучением, когда они поднимаются в стратосферу. В конце 1973, Роуленд и Молина, которые недавно присоединились к лаборатории Роуленда, использовали данные из различных опубликованных источников, чтобы рассчитать, что молекулы ХФУ, выпущенные вблизи поверхности Земли, спустя десятилетия окажутся в стратосфере, где УФ-излучение отщепит атомы хлора. Каждый атом хлора немедленно прореагирует с молекулой озона, запустив цепную реакцию, которая уничтожит тысячи молекул озона. В своей статье они подсчитали, что если немедленно запретить использование ХФУ, потеря озона будет продолжаться в течение многих лет. Однако, если производство ХФУ продолжится, потери озона будут еще больше.
Каждый атом хлора немедленно прореагирует с молекулой озона, запустив цепную реакцию, которая уничтожит тысячи молекул озона. В своей статье они подсчитали, что если немедленно запретить использование ХФУ, потеря озона будет продолжаться в течение многих лет. Однако, если производство ХФУ продолжится, потери озона будут еще больше.
«Когда мы поняли, что существует очень эффективная цепная реакция, которая превратила исследование CFC из интересной научной проблемы в проблему, имеющую серьезные экологические последствия», — сказал Роуленд Chemical & Engineering News в обширном интервью в 2007 году. «Вы не часто чувствуете мурашки по спине, когда смотрите на научные результаты», — добавил он, но это был один из тех моментов.
К началу страницы
От исследований к сопротивлению
В 1976 году Национальная академия наук выпустила отчет, подтверждающий разрушительное воздействие ХФУ на стратосферный озон. Слушания в Конгрессе пришли к аналогичным выводам, и штаты и федеральное правительство начали изучать запреты на использование ХФУ в аэрозольных баллончиках. Химическая промышленность утверждала, что данные о фреонах и стратосферном озоне неубедительны и не требуют решительных действий. Когда Роуленд читал лекции о ХФУ, отраслевые группы часто делали заявления, оспаривающие его заявления. Как вспоминает сегодня Молина, «Шерри [Роуленд] была авторитетным и уважаемым ученым, регулярно выступавшим с докладами по всему миру. Казалось, что из-за того, что он сосредоточился на ХФУ и разрушении озонового слоя, он стал получать меньше приглашений выступить. Это беспокоило его».
Химическая промышленность утверждала, что данные о фреонах и стратосферном озоне неубедительны и не требуют решительных действий. Когда Роуленд читал лекции о ХФУ, отраслевые группы часто делали заявления, оспаривающие его заявления. Как вспоминает сегодня Молина, «Шерри [Роуленд] была авторитетным и уважаемым ученым, регулярно выступавшим с докладами по всему миру. Казалось, что из-за того, что он сосредоточился на ХФУ и разрушении озонового слоя, он стал получать меньше приглашений выступить. Это беспокоило его».
Роуленд, Молина и другие ученые, пытавшиеся понять химию стратосферы, столкнулись с серьезными и фундаментальными проблемами. Во взаимодействии ХФУ и озона в стратосфере явно участвовало значительное число химических соединений. Большинство из них очень реакционноспособны и присутствуют только в следовых количествах. Их химию было трудно воспроизвести в лаборатории.
Кроме того, концентрации стратосферного озона естественным образом колеблются в зависимости от географического положения и сезона. Стратосфера — непростое место для проведения исследований. Измерения концентрации озона проводились приборами, доставляемыми в стратосферу воздушными шарами и самолетами. Озон также измерялся приборами на спутниках, вращающихся вокруг Земли, хотя спутниковая технология в середине 1970-е были еще довольно примитивными.
Стратосфера — непростое место для проведения исследований. Измерения концентрации озона проводились приборами, доставляемыми в стратосферу воздушными шарами и самолетами. Озон также измерялся приборами на спутниках, вращающихся вокруг Земли, хотя спутниковая технология в середине 1970-е были еще довольно примитивными.
Все эти неопределенности дали критикам гипотезы Роуленда и Молины много материала для работы. Они очень убедительно доказывали многим, что просто не имеет смысла принимать меры против класса очень полезных химических веществ на основании таких надуманных доказательств. Промышленные критики, в частности, утверждали, что одно дело предложить поэтапный отказ от использования ХФУ в качестве пропеллента в аэрозольных баллончиках — относительно тривиальное использование соединений, — и совсем другое — рассмотреть вопрос о запрете их использования в холодильниках и кондиционерах, где в то время просто не существовало очевидных альтернатив ХФУ.
К началу страницы
Антарктическая озоновая дыра
Важнейшие доказательства, подтверждающие гипотезу ХФУ, были получены от британских ученых, работающих на станции Галлей-Бей Британской антарктической службы, которые десятилетиями проводили наземные измерения общего содержания озона. В 1984 г. Джозеф С. Фарман (1930–2013 гг.) и его коллеги из BAS изучили необработанные данные и обнаружили, что содержание стратосферного озона значительно уменьшилось с 1960-х годов. В 1985 году ученые опубликовали в журнале Nature статью, в которой сообщалось, что в сентябре, в конце южной зимы, стратосферный озон над Антарктидой уменьшился на 40%.
В 1984 г. Джозеф С. Фарман (1930–2013 гг.) и его коллеги из BAS изучили необработанные данные и обнаружили, что содержание стратосферного озона значительно уменьшилось с 1960-х годов. В 1985 году ученые опубликовали в журнале Nature статью, в которой сообщалось, что в сентябре, в конце южной зимы, стратосферный озон над Антарктидой уменьшился на 40%.
Антарктическая озоновая дыра, как ее стали называть, сделала разрушение озонового слоя реальной и настоящей опасностью для законодателей и широкой общественности. Прогнозы значительного увеличения заболеваемости раком кожи в результате продолжающегося использования ХФУ стимулировали международные действия. В 1987 году 56 стран согласились в соответствии с так называемым Монреальским протоколом сократить производство и использование ХФУ вдвое. В последующие годы протокол был усилен, чтобы потребовать постепенного прекращения производства ХФУ и других озоноразрушающих веществ во всем мире.
В результате работы Роуленда и Молины люди впервые осознали, что их деятельность может влиять на окружающую среду Земли в планетарном масштабе. Как говорит сегодня Молина: «Неважно, где происходят выбросы ХФУ. Это глобальная проблема. Важно то, что это привело к международному соглашению, которое решило проблему». Сага о ХФУ и озоновом слое содержит много уроков для человечества, сталкивающегося с еще более серьезной проблемой глобального изменения климата.
Как говорит сегодня Молина: «Неважно, где происходят выбросы ХФУ. Это глобальная проблема. Важно то, что это привело к международному соглашению, которое решило проблему». Сага о ХФУ и озоновом слое содержит много уроков для человечества, сталкивающегося с еще более серьезной проблемой глобального изменения климата.
К началу страницы
Помимо работы, получившей Нобелевскую премию и показывающей, что ХФУ разрушают озоновый слой Земли, Роуленд и Молина сыграли ключевую роль в убеждении ученых, политиков и широкой общественности в вредном воздействии ХФУ. Их беспрецедентная пропаганда в конечном итоге привела к поэтапному отказу от ХФУ во всем мире благодаря принятию Монреальского протокола в 1987 году. Исследования Роуленда и Молины привлекли внимание всего мира к воздействию антропогенного загрязнения в планетарном масштабе. Их работа была одной из первых, которые напрямую повлияли на глобальный сдвиг в политике, предшествовавший нынешним дебатам об изменении климата».
— Кеннет К. Джанда, профессор химии и декан Школы физических наук Калифорнийского университета в Ирвине Национальная историческая химическая достопримечательность на церемонии в Калифорнийском университете в Ирвине 18 апреля 2017 года. На памятной доске написано:
Джанда, профессор химии и декан Школы физических наук Калифорнийского университета в Ирвине Национальная историческая химическая достопримечательность на церемонии в Калифорнийском университете в Ирвине 18 апреля 2017 года. На памятной доске написано:
. Когда ученые сообщили о своих открытиях в 1974, ХФУ широко использовались в качестве газообразных хладагентов и в качестве пропеллентов в аэрозольных распылителях. Роуленд и Молина убедили скептически настроенных промышленников, политиков и общественность в опасности ХФУ. Активность ученых — и открытие другими исследователями того, что озоновый слой над Антарктикой истончается, — привели к поэтапному отказу от ХФУ во всем мире и разработке более безопасных альтернатив. За свою работу Роуленд и Молина разделили Нобелевскую премию по химии 1995 года с другим атмосферным химиком, Полом Дж. Крутценом.
Благодарности
Адаптировано для Интернета из документа «Хлорфторуглероды и разрушение озонового слоя», подготовленного Американским химическим обществом в рамках программы «Национальные исторические химические достопримечательности» в 2017 г.
К началу страницы
Дополнительные ресурсы
План
Дополнительная литература
- Документ Molina & Rowland 1974 г. «Стратосферный поглотитель хлорфторуглеродов: разрушение озона, катализируемое атомами хлора» Природа 249 (5460), 810-812
- Марио Молина, заслуженный профессор химии и биохимии, Калифорнийский университет, Сан-Диего
- Пресс-релиз Нобелевской премии по химии 1995 г.
- Монреальский протокол (через EPA.gov)
- Статья Роуленда об исследованиях, приносящих пользу человечеству (через Национальные академии)
- Нобелевская лекция Роуленда по химии, 8 декабря 1995 г. (через NobelPrize.org)
- Молина Нобелевская лекция по химии, 8, 19 декабря95 (через NobelPrize.org)
- На испанском языке: Лос-хлорофторуглерод и эль-агуеро де озоно
Цитировать эту страницу
Американское химическое общество National Historic Chemical Landmarks.
